题目内容
【题目】A、B、C、D、E是中学化学中常见的四种短周期元素,有关位置及信息如下:
A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质一般保存在煤油中;F单质是日常生活中用量最大的金属,易被腐蚀或损坏。
| E | A | B | ||
C |
| D |
请回答下列问题:
![]() 元素的氢化物水溶液能使酚酞变红的原因用电离方程式解释为 ______ 。
元素的氢化物水溶液能使酚酞变红的原因用电离方程式解释为 ______ 。
![]() 、D的氢化物相互反应,产生白色固体,鉴定该固体需用到的试剂或试纸
、D的氢化物相互反应,产生白色固体,鉴定该固体需用到的试剂或试纸![]() 蒸馏水除外
蒸馏水除外![]() 有 ______ 。
有 ______ 。
![]() 、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为 ______ 。
、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为 ______ 。
![]() 与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有: ______ 。
与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有: ______ 。
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
![]() 和C组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是 ______ 。
和C组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是 ______ 。
![]() 已知一定量的E单质能在
已知一定量的E单质能在![]()
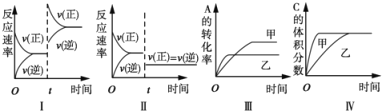
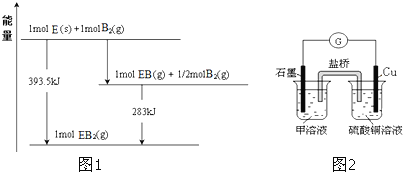
![]() 中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下
中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下![]() 与
与![]() 反应生成
反应生成![]() 的热化学方程式 ______ 。
的热化学方程式 ______ 。
![]() 若在D与F组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极出现的现象是 ______ ,负极的反应式为 ______ 。
若在D与F组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极出现的现象是 ______ ,负极的反应式为 ______ 。
【答案】![]() 氢氧化钠溶液、红色石蕊试纸,硝酸银溶液、稀硝酸 离子键和共价键 ①③④
氢氧化钠溶液、红色石蕊试纸,硝酸银溶液、稀硝酸 离子键和共价键 ①③④ ![]()
![]() ;
;![]() 黄色溶液慢慢变为浅绿色
黄色溶液慢慢变为浅绿色 ![]()
【解析】
A、B、C、D、E是中学化学中常见的四种短周期元素,A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物,该离子化合物为铵盐,则A为N元素;C单质一般保存在煤油中,则C为Na;F单质是日常生活中用量最大的金属,易被腐蚀或损坏,则F为Fe;由元素在周期表中的相对位置可知,E为C元素、B为O元素,D为Cl元素;
![]() 为N元素,其氢化物
为N元素,其氢化物![]() 水溶液中一水合氨发生电离:
水溶液中一水合氨发生电离:![]() ,溶液呈碱性,能使酚酞变红,故答案为:
,溶液呈碱性,能使酚酞变红,故答案为:![]() ;
;
![]() 、D的氢化物相互反应,产生白色固体为
、D的氢化物相互反应,产生白色固体为![]() ,检验铵根离子用氢氧化钠和红色石蕊试纸,检验氯离子用稀硝酸和硝酸银;故答案为:氢氧化钠溶液、红色石蕊试纸,硝酸银溶液、稀硝酸;
,检验铵根离子用氢氧化钠和红色石蕊试纸,检验氯离子用稀硝酸和硝酸银;故答案为:氢氧化钠溶液、红色石蕊试纸,硝酸银溶液、稀硝酸;
![]() 、C组成的化合物
、C组成的化合物![]() 和
和![]() 反应可生成
反应可生成![]() ,
,![]() 中所含有的化学键为离子键和共价键;故答案为:离子键和共价键;
中所含有的化学键为离子键和共价键;故答案为:离子键和共价键;
![]() 与O可组成质量比为7:16的三原子分子,分子中N原子与氧原子数目之比
与O可组成质量比为7:16的三原子分子,分子中N原子与氧原子数目之比![]() :
:![]() :2,该分子为
:2,该分子为![]() ,该分子释放在空气中其化学作用可能引发的后果有:酸雨、光化学烟雾、破坏臭氧层,二氧化碳等为导致温室效应,故答案为:
,该分子释放在空气中其化学作用可能引发的后果有:酸雨、光化学烟雾、破坏臭氧层,二氧化碳等为导致温室效应,故答案为:![]() ;
;
![]() 和Na组成的一种离子化合物,能与水反应生成两种碱,该化合物为
和Na组成的一种离子化合物,能与水反应生成两种碱,该化合物为 ,该反应的化学方程式是:
,该反应的化学方程式是:![]() ,故答案为:
,故答案为:![]() ;
;
![]() 由图可知,
由图可知,![]() 与
与![]() 反应得到
反应得到![]() 放出热量
放出热量![]() ,该反应热化学方程式为:
,该反应热化学方程式为:![]() 与
与![]() 反应得到
反应得到![]() 放出热量
放出热量![]() ,该反应热化学方程式为:
,该反应热化学方程式为:![]() 根据盖斯定律,
根据盖斯定律,![]() 得:
得:![]() ,故答案为:
,故答案为:![]() ;
;
![]() 若在Cl与Fe组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,则甲为
若在Cl与Fe组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,则甲为![]() ,两者反应的方程式为Cu+2FeCl3=CuCl2+2FeCl2,设计如图所示的原电池,正极上
,两者反应的方程式为Cu+2FeCl3=CuCl2+2FeCl2,设计如图所示的原电池,正极上![]() 黄色
黄色![]() 得电子生成
得电子生成![]() 浅绿色
浅绿色![]() ,则正极出现的现象是黄色溶液慢慢变为浅绿色,负极反应式为:
,则正极出现的现象是黄色溶液慢慢变为浅绿色,负极反应式为:![]() ,故答案为:黄色溶液慢慢变为浅绿色;
,故答案为:黄色溶液慢慢变为浅绿色;![]() 。
。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】在不同温度下,向 2 L密闭容器中加入1 mol NO(g)和1 mol活性炭(C),发生反应:2NO(g)+C(s) ![]() N2(g)+CO2(g) ΔH=-213.5 kJ·mol-1,达到平衡时的数据如下。
N2(g)+CO2(g) ΔH=-213.5 kJ·mol-1,达到平衡时的数据如下。
温度/℃ | n(C)/mol | n(CO2)/mol |
t1 | 0.70 | |
t2 | 0.25 |
下列说法不正确的是( )
A.上述信息可推知:t1<t2
B.t1℃ 时,该反应的平衡常数K=![]()
C.t2℃ 时,若反应达平衡后再缩小容器的容积,c(N2)∶c(NO)不变
D.t1℃ 时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小