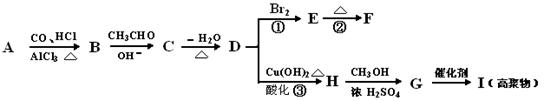
题目内容
甲醇(CH3OH)可以与水蒸气反应生成氢气,反应方程式如下:CH3OH(g)+H2O(g)?CO2(g)+3H2(g)
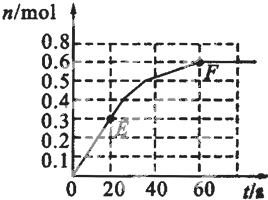
一定条件下,向体积为2L的恒容密闭容器中充入1molCH3OH(g)和3molH2O(g),20s后达到平衡,测得混合气体的压强是反应前的1.2倍.
(1)20s中用甲醇表示的该反应的平均速率为多少?
(2)甲醇的平衡转化率为多少?
一定条件下,向体积为2L的恒容密闭容器中充入1molCH3OH(g)和3molH2O(g),20s后达到平衡,测得混合气体的压强是反应前的1.2倍.
(1)20s中用甲醇表示的该反应的平均速率为多少?
(2)甲醇的平衡转化率为多少?
根据压强之比等于物质的量之比,故反应后混合气体总的物质的量=1.2×(1mol+3mol)=4.8mol,
令参加反应的甲醇的物质的量为xmol,则:
CH3OH(g)+H2O(g)?CO2(g)+3H2(g) 物质的量增大△n
1 2
xmol 4.8mol-4mol=0.8mol
故x=0.4mol
(1)v(CH3OH)=
=0.01mol/(L?s),
答:20s中用甲醇表示的该反应的平均速率为0.01mol/(L?s).
(2)甲醇的转化率=
×100%=40%,
答:甲醇的转化率为40%.
令参加反应的甲醇的物质的量为xmol,则:
CH3OH(g)+H2O(g)?CO2(g)+3H2(g) 物质的量增大△n
1 2
xmol 4.8mol-4mol=0.8mol
故x=0.4mol
(1)v(CH3OH)=
| ||
| 20s |
答:20s中用甲醇表示的该反应的平均速率为0.01mol/(L?s).
(2)甲醇的转化率=
| 0.4mol |
| 1mol |
答:甲醇的转化率为40%.

练习册系列答案
相关题目
 z C(g)的反应达到平衡。
z C(g)的反应达到平衡。