题目内容
13.NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 0.5mol/L的Ba(0H)2溶液中0H一的数目为NA | |
| B. | 1 mol FeI2与足量氯气反应时转移的电子数为2NA | |
| C. | 1.6gNH2-离子所含质子数为NA | |
| D. | 92g NO2和N204混合气体中含有的原子数为6NA |
分析 A、溶液体积不明确;
B、1 mol FeI2中含1mol亚铁离子和2mol碘离子;
C、求出NH2-离子的物质的量,然后根据1molNH2-离子中含9mol质子来分析;
D、NO2和N204的最简式均为NO2.
解答 解:A、溶液体积不明确,故溶液中的氢氧根的物质的量无法计算,故A错误;
B、1 mol FeI2中含1mol亚铁离子和2mol碘离子,均能被氯气氧化为铁离子和碘单质,故1mol1 mol FeI2失去3mol电子,即3NA个,故B错误;
C、1.6gNH2-离子的物质的量为0.1mol,而1molNH2-离子中含9mol质子,故0.1molNH2-中含0.9mol质子即0.9NA个,故C错误;
D、NO2和N204的最简式均为NO2,故92gNO2和N204中含有的NO2的物质的量为n=$\frac{92g}{46g/mol}$=2mol,故含6mol原子即6NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
16.将4.6g钠和4.8g镁分别投入盛有等物质的量浓度、等体积的稀硫酸的两个烧杯中,反应后溶液质量分别为m g和n g,则不可能的关系为( )
| A. | m=n | B. | m>n | C. | m<n | D. | m≤n |
8.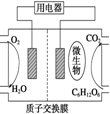 生物体中细胞膜内的葡萄糖,细胞膜外的富氧液体及细胞膜构成微型的生物原电池,下列有关判断正确的是( )
生物体中细胞膜内的葡萄糖,细胞膜外的富氧液体及细胞膜构成微型的生物原电池,下列有关判断正确的是( )
 生物体中细胞膜内的葡萄糖,细胞膜外的富氧液体及细胞膜构成微型的生物原电池,下列有关判断正确的是( )
生物体中细胞膜内的葡萄糖,细胞膜外的富氧液体及细胞膜构成微型的生物原电池,下列有关判断正确的是( )| A. | 正极的电极反应式可能是O2+4e-═2O2- | |
| B. | 负极的电极反应式可能是O2+4e-+2H2O═4OH- | |
| C. | 正极反应主要是C6H12O6生成CO2或HCO3- | |
| D. | 负极反应主要是C6H12O6生成CO2或HCO3- |
5.下列反应的离子方程式正确的是( )
| A. | 碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| B. | 25mL 0.3mol•L-1的FeBr2溶液中通入224mL标准状况下的氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| C. | 100mL 0.1mol•L-1的Al2(SO4)3溶液中加入20mL 3.5mol•L-1的NaOH溶液:Al3++4OH-═[Al(OH)4]- | |
| D. | 过量铁粉和稀硝酸反应:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
3.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,3.2 g O2所含氧原子的数目为0.2 NA | |
| B. | 含有NA个阴离子的Na2O2与足量水反应,转移电子数为2NA | |
| C. | 标准状况下,等体积的水和CO2,含有的氧原子数目为1:2 | |
| D. | 1L 1mol/L饱和FeCl3滴入沸水中完全水解生成Fe(OH)3胶体粒子个数为NA个 |
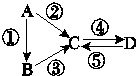 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系: A、B、C、D、E、F为原子序数依次增大的短周期元素,G为第四周期元素,B、C相邻且同周期,A、D同主族.A、C能形成两种化合物甲和乙,原子个数比分别为2:1和1:1,甲为常见的溶剂.E是地壳中含量最多的金属元素.F元素为同周期电负性最大的元素.D和F可形成化合物丙,E和F可形成化合物丁.G为第四周期未成对电子数最多的元素.请回答下列问题:
A、B、C、D、E、F为原子序数依次增大的短周期元素,G为第四周期元素,B、C相邻且同周期,A、D同主族.A、C能形成两种化合物甲和乙,原子个数比分别为2:1和1:1,甲为常见的溶剂.E是地壳中含量最多的金属元素.F元素为同周期电负性最大的元素.D和F可形成化合物丙,E和F可形成化合物丁.G为第四周期未成对电子数最多的元素.请回答下列问题: