题目内容
【题目】一定温度下,BaSO4(s)![]() Ba2+(aq) + SO42-(aq)体系中, c(Ba2+)和c(SO42-)关系如图所示。下列说法正确的是
Ba2+(aq) + SO42-(aq)体系中, c(Ba2+)和c(SO42-)关系如图所示。下列说法正确的是
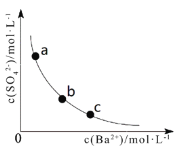
A.a、b、c三点对应的Ksp相等
B.BaSO4在c点的溶解度比b点的大
C.BaSO4溶于水形成的饱和溶液中,c(Ba2+)=c(SO42-)
D.b点的溶液中加入BaCl2固体,c(SO42-)沿曲线向a点方向变化
【答案】AC
【解析】
A. a、b、c三点为曲线上的点,温度未变则三点对应的Ksp相等,A正确;
B. BaSO4在c点的c(SO42-)< c(Ba2+),且小于b点,则溶解度比b点的小,B错误;
C. BaSO4溶于水形成的饱和溶液中,c(Ba2+)=c(SO42-),C正确;
D. b点的溶液中加入BaCl2固体,溶液中c(Ba2+)增大,则c(SO42-)沿曲线向从点方向变化,D错误;
答案为AC。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
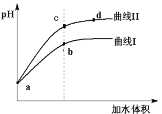
【题目】已知T ℃时两种弱酸的电离平衡常数如下表。将pH和体积均相同的两种酸溶液M、N分别稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
弱酸 | HNO2 | CH3COOH |
电离平衡常数 | 5.0×10-4 | 1.7×10-5 |
A.曲线Ⅰ代表CH3COOH溶液
B.M、N两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
C.溶液中水的电离程度:b点<c点
D.从c点到d点,溶液中 保持不变(其中HA、A-分别代表相应的酸和酸根离子)
保持不变(其中HA、A-分别代表相应的酸和酸根离子)