题目内容
1.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 1 molCaC2晶体中含有的离子总数为3NA | |
| B. | 常温常压下,3g-CH3中含有的电子数为1.8NA | |
| C. | NA个HCl分子与22.4LH2和Cl2的混合气体所含有的原子数均为2NA | |
| D. | 80 mL 12 mol/L的浓盐酸与足量MnO2反应,生成的Cl2分子数目为0.48 NA |
分析 A、CaC2是Ca2+和C22-离子构成;
B、甲基是中性原子团,n=$\frac{m}{M}$计算物质的量,结合甲基取代基计算所含电子数;
C、温度压强不知,22.4LH2和Cl2的混合气体物质的量不能计算;
D、浓盐酸与足量MnO2反应,随反应进行,浓盐酸变化为稀盐酸后不能和二氧化锰继续反应生成氯气;
解答 解:A、CaC2是Ca2+和C22-离子构成,1 molCaC2晶体中含有的离子总数为2NA,故A错误;
B、甲基是中性原子团,n=$\frac{m}{M}$计算物质的量=$\frac{3g}{15g/mol}$=0.2mol,结合甲基取代基计算所含电子数=0.2mol×9×NA=1.8NA,故B正确;
C、温度压强不知,22.4LH2和Cl2的混合气体物质的量不能计算,故C错误;
D、浓盐酸与足量MnO2反应,随反应进行,浓盐酸变化为稀盐酸后不能和二氧化锰继续反应生成氯气,生成的Cl2分子数目小于0.48 NA,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用,物质结构的分析判断,物质的量计算应用,掌握基础是关键,题目较简单.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
12.25℃时,NH3•H2O和CH3COOH的电离常数K相等.下列说法正确的是( )
| A. | 常温下,CH3COONH4溶液的pH=7,与纯水中H2O的电离程度相同 | |
| B. | 向CH3COONH4溶液加入CH3COONa固体时,c(NH4+)、c(CH3COO-)均会增大 | |
| C. | 常温下,等浓度的NH4Cl和CH3COONa两溶液的pH之和为14 | |
| D. | 等温等浓度的氨水和醋酸两溶液加水稀释到相同体积,溶液pH的变化值一定相同 |
9.为了更好的解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻找新能源.对以下做法的描述不正确的是( )
| A. | 为了使燃料充分燃烧,通入的空气要适当过量 | |
| B. | 目前锅炉燃烧采用沸腾炉的逐渐增多,目的是提高煤炭的热效率并减少SO2的排放 | |
| C. | 为提高热能的利用率,可以在煤燃烧后排放废气的烟道中安装热交换装置 | |
| D. | 为开发氢能,可研究设法将太阳能聚焦,产生高温使水分解产生氢气 |
6.下列有关说法正确的是( )
| A. | 通式相同的两种有机物按不同比例混合时,只要总质量一定,完全燃烧的耗氧量就一定 | |
| B. | 除去甲烷中的乙烯可用溴水或酸性高锰酸钾溶液 | |
| C. | 糖类、油脂、蛋白质都会在一定条件下水解 | |
| D. | 戊烷有3种同分异构体,而一氯戊烷有8种同分异构体 |
6.HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是( )
| A. | 0.1mol•L-1 HA 中c(H+)=c(OH-)+c(A-), | |
| B. | 0.1mol•L-1 HA 与 0.1 mol•L-1NaOH 混合至溶液呈中性:c(Na+)<c(A-) | |
| C. | 0.1mol•L-1 NaA 中c(Na+)>c(OH-)>c(A-)>c(H+) | |
| D. | 0.1mol•L-1 HA中加入少量NaA固体,HA的电离常数减小 |
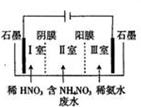 硝酸铵钙[5Ca(NO3)2•NH4NO3•10H2O]极易溶于水,是一种绿色复合肥料.
硝酸铵钙[5Ca(NO3)2•NH4NO3•10H2O]极易溶于水,是一种绿色复合肥料.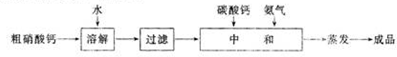
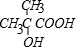 ;b 的结构简式
;b 的结构简式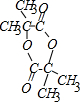 .
.