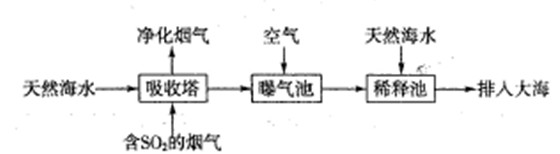
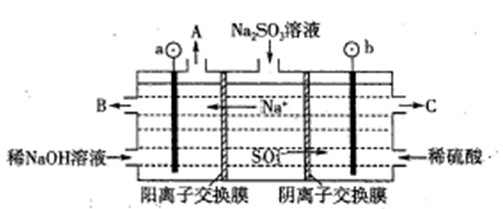
题目内容
(1)为了证明一水合氨是弱碱,甲、乙、丙三同学分别设计以下实验进行探究。
①甲同学用pH试纸测得室温下0.10 mol·L-1氨水pH为10,则认定一水合氨是弱电解质,理由是 。
②乙同学取10 mL 0.10 mol·L-1氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000 mL,再用pH试纸测出其pH为b,若要确认一水合氨是弱电解质,则a、b应满足的关系是 (用等式或不等式表示)。
③丙同学取出10 mL 0.10mol·L-1氨水,滴入2滴酚酞试液,显粉红色,再加入NH4Cl晶体少量,观察到的现象是 ,则证明—水合氨是弱电解质。
(2)向25 mL 0.10 mol·L-l的盐酸中滴加氨水至过量,该过程中离子浓度大小关系可能正确的是 。
a.c(C1-)=c(NH4+)>c(H+)=c(OH-) b.c(C1-)>c(NH4+)=c(H+)>c(OH-)
c.c(NH4+)>c(OH-)>c(C1-)>c(H+) d.c(OH-)>c(NH4+)>c(H+)>c(C1-)
(3)常温下,0.10mol·L-l的NH4Cl溶液pH为5,则一水合氨的电离常数Kb= 。
(1) ①如果氨水是强碱,0.10mol?L-1氨水pH为13,溶液的pH=10<13,所以一水合氨是弱碱;②(a-2)<b<a;③溶液的颜色变浅;
(2)abc;(3)1×10—5。
解析试题分析:(1)若证明一水合氨是弱碱,需从以下几个角度考虑:a、看电离程度b、看是否存在电离平衡c、测盐溶液的pH。 ①甲同学用pH试纸测得室温下0.10 mol·L-1氨水pH为10,则认定一水合氨是弱电解质,理由是如果氨水是强碱,0.10mol?L-1氨水pH为13,溶液的pH=10<13,所以一水合氨是弱碱;②若是强碱,稀释100倍,pH减小2个单位,由于一水合氨是弱碱,稀释的过程中,促进电离,c(OH-)变化的幅度变小,pH减小幅度小于2个单位,则有a-2<b,且b<a;答案为:(a-2)<b<a;③如果一水合氨是弱碱,则存在电离平衡NH3·H2O  NH4+ + OH-,向氨水中加入氯化铵后,铵离子浓度增大,平衡逆向移动,溶液中氢氧根离子浓度降低,溶液的碱性减弱,则溶液的颜色变浅;(2)向25 mL 0.10 mol·L-l的盐酸中滴加氨水至过量,a.氨水稍过量,混合液呈中性,c(C1-)=c(NH4+)>c(H+)=c(OH-) ,正确;b.盐酸过量,溶液为盐酸和氯化铵的混合液,溶液显酸性,c(C1-)>c(NH4+)=c(H+)>c(OH-),正确;c.氨水远远过量,溶液为氨水和氯化铵的混合液,一水合氨的电离程度大于铵离子的水解程度,溶液呈碱性,c(NH4+)>c(OH-)>c(C1-)>c(H+),正确;d.不可能出现c(OH-)>c(NH4+)>c(H+)>c(C1-),错误;选abc; (3)常温下,0.10mol·L-l的NH4Cl溶液pH为5,NH4+的水解常数Kh=[H+][NH3·H2O]/[NH4+]=10—9,水合氨的电离常数
NH4+ + OH-,向氨水中加入氯化铵后,铵离子浓度增大,平衡逆向移动,溶液中氢氧根离子浓度降低,溶液的碱性减弱,则溶液的颜色变浅;(2)向25 mL 0.10 mol·L-l的盐酸中滴加氨水至过量,a.氨水稍过量,混合液呈中性,c(C1-)=c(NH4+)>c(H+)=c(OH-) ,正确;b.盐酸过量,溶液为盐酸和氯化铵的混合液,溶液显酸性,c(C1-)>c(NH4+)=c(H+)>c(OH-),正确;c.氨水远远过量,溶液为氨水和氯化铵的混合液,一水合氨的电离程度大于铵离子的水解程度,溶液呈碱性,c(NH4+)>c(OH-)>c(C1-)>c(H+),正确;d.不可能出现c(OH-)>c(NH4+)>c(H+)>c(C1-),错误;选abc; (3)常温下,0.10mol·L-l的NH4Cl溶液pH为5,NH4+的水解常数Kh=[H+][NH3·H2O]/[NH4+]=10—9,水合氨的电离常数
Kb=[OH-][NH4+]/[NH3·H2O]=Kw/Kh=1×10—5。
考点:考查强弱电解质的比较、酸碱混合溶液中离子浓度大小比较及电离平衡常数计算。

复分解反应是中学化学中常见的一种反应类型。
(1)已知在常温下测得浓度均为0.1 mol·L-1的下列6种溶液的pH(C6H5OH相当于一元弱酸):
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
复分解存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O。若换个角度看,它同时揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该规律,请判断下列反应不能成立的是______________(填编号)。
A.CO2+H2O+2NaClO=Na2CO3+2HClO
B.CO2+H2O+NaClO=NaHCO3+HClO
C.CO2+H2O+C6H5ONa―→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa―→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH―→NaHCO3+C6H5ONa
F.CH3COOH+NaCN=CH3COONa+HCN
(2)根据前述信息判断,浓度均为0.05 mol·L-1的下列六种物质的溶液中,pH最小的是________(填编号);其pH等于________(填数值);pH最大的是________(填编号)。
①C6H5OH ②CH3COOH ③HCN ④HClO
⑤H2SO4 ⑥HClO4
(3)一些复分解反应的发生还遵循其他的规律。下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性钠溶液
②侯氏制碱法中,向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打晶体
③蒸发KCl和NaNO3混合溶液,首先析出NaCl晶体根据上述反应,总结出复分解反应发生的另一规律___________________________________________
将KI溶液和AgCl固体混合搅拌,会观察到的现象是____________________________________,请写出反应的离子方程式______________________________________________
(1)将0.15 mol·L-1稀硫酸V1 mL与0.1 mol·L-1 NaOH溶液V2 mL混合,所得溶液的pH为1,则V1:V2=________。(溶液体积变化忽略不计)
(2)常温下,某水溶液中存在的离子有:Na+、A-、H+、OH-,据题意,回答下列问题:
①若该水溶液由0.1 mol·L-1 HA溶液与0.1 mol·L-1NaOH溶液等体积混合而得,则溶液的pH________7。
②若溶液pH>7,则c(Na+)________c(A-),理由是________。
③若该溶液由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2 mL混合而得,则下列说法正确的是________。
| A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol·L-1 |
| B.若V1=V2,反应后溶液pH一定等于7 |
| C.若反应后溶液呈酸性,则V1一定大于V2 |
| D.若反应后溶液呈碱性,则V1一定小于V2 |
利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下:
已知:Zn及其化合物的性质与Al及其化合物的性质相似,请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用有________。
| A.去除油污 | B.溶解镀锌层 | C.去除铁锈 | D.钝化 |
(3)由溶液B制取Fe3O4胶体粒子的过程中,须持续通入N2,其原因是
_______________________________________________________________
(4)Fe3O4胶体粒子能否用减压过滤法实现固液分离?__________(填“能”或“不能”),理由是________________________________。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.010 00 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取________ g K2Cr2O7(保留4位有效数字,已知MK2Cr2O7=294.0 g·mol-1)。配制该标准溶液时,下列仪器中不必要用到的有________(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒
⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6) 滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将________(填“偏大”、“偏小”或“不变”)。
已知25 ℃时部分弱电解质的电离平衡常数数据如表所示: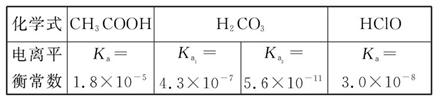
回答下列问题:
(1)物质的量浓度均为0.1 mol·L-1的四种溶液:
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大排列顺序是 (用编号填写)。
(2)常温下,0.1 mol/L的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 。
| A.c(H+) |
| B.c(H+)/c(CH3COOH) |
| C.c(H+)·c(OH-) |
| D.c(OH-)/c(H+) |
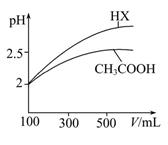
(3)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数 (填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数,理由是 。
25 ℃时,用浓度为0.100 0 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L-1的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是 ( )。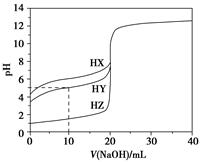
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX |
| B.根据滴定曲线,可得Ka(HY)≈10-5 |
| C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) |
D.HY与HZ混合,达到平衡时c(H+)= +c(Z-)+c(OH-) +c(Z-)+c(OH-) |
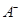 离子数目变化趋势的是 (填字母)。
离子数目变化趋势的是 (填字母)。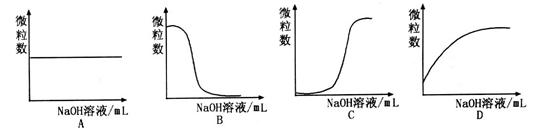
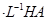 溶液和1体积0.02mol
溶液和1体积0.02mol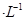 NaOH溶液混合,得到2体积混合溶液。
NaOH溶液混合,得到2体积混合溶液。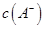 0.01 mol
0.01 mol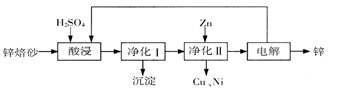
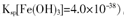 。
。