题目内容
9.在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是( )| A. | v(NH3)=0.3 mol/(L•min) | B. | v(N2)=0.01 mol/(L•s) | ||
| C. | v(N2)=0.2 mol/(L•min) | D. | v(H2)=0.3 mol/(L•min) |
分析 不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意保持单位一致.
解答 解:不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,对于N2+3H2?2NH3,
A.$\frac{v(N{H}_{3})}{2}$=0.15 mol/(L•min);
B.v(N2)=0.01 mol/(L•s)=0.6 mol/(L•min),$\frac{v({N}_{2})}{1}$=0.6 mol/(L•min);
C.$\frac{v({N}_{2})}{1}$=0.1 mol/(L•min);
D.$\frac{v({H}_{2})}{3}$=0.1 mol/(L•min),
故反应速率B>A>C=D,
故选B.
点评 本题考查化学反应速率快慢比较,难度不大,可以转化为同一物质表示的速率比较,利用比值法可以快速判断,注意单位保持一致.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
19.短周期元素X和Y,X原子的电子层数为n,最外层电子数为(2n+1),Y原子最外层电子数是次外层电子数的3倍.下列说法一定正确的是( )
| A. | X和Y都是非金属元素,其中X的最高化合价为+5价 | |
| B. | X与Y所能形成的化合物都是酸性氧化物 | |
| C. | 元素X的氧化物的水化物是强酸 | |
| D. | X的氢化物极易溶于水,可以用来做喷泉实验 |
20. 某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述不正确的是( )
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述不正确的是( )
 某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述不正确的是( )
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述不正确的是( )| A. | 1mol该物质完全燃烧最多能消耗10.5mol的氧气 | |
| B. | 能使酸性KMnO4溶液褪色 | |
| C. | 1mol该物质最多能与4 molH2加成 | |
| D. | 分子式为C10H9O3 |
17.设nA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 1mol Fe与足量的盐酸反应,转移3nA个电子 | |
| B. | 0.1mol•L-1的NaNO3溶液中含有0.1nA个NO3- | |
| C. | 常温下,34gNH3含有2nA个NH3分子 | |
| D. | 常温常压下,22.4LNO2含有2nA个氧原子 |
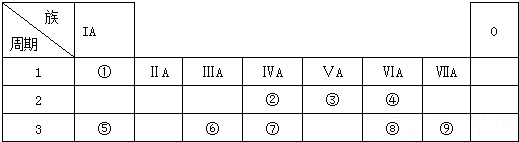
14.下表是周期表的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答问题:
(1)表中元素,化学性质最不活泼的是Ar,只有负价而无正价的是F,可用于制半导体材料的元素是Si.
(2)最高价氧化物的水化物碱性最强的物质的电子式是 ,酸性最强的物质是HClO4,呈两性的物质是Al(OH)3;
,酸性最强的物质是HClO4,呈两性的物质是Al(OH)3;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的化合物是HF;
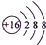
(4)B元素与A形成的化合物和水反应后溶液呈碱性,同时生成一种可燃气体,写出反应的化学方程式NaH+H2O=NaOH+H2↑.
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(2)最高价氧化物的水化物碱性最强的物质的电子式是
 ,酸性最强的物质是HClO4,呈两性的物质是Al(OH)3;
,酸性最强的物质是HClO4,呈两性的物质是Al(OH)3;(3)A分别与D、E、F、G、H形成的化合物中,最稳定的化合物是HF;
(4)B元素与A形成的化合物和水反应后溶液呈碱性,同时生成一种可燃气体,写出反应的化学方程式NaH+H2O=NaOH+H2↑.
19.与CH2=CH2→CH2Br-CH2Br的变化属于同一反应类型的是( )
| A. | CH3CHO→C2H5OH | B. | C2H5Cl→CH2=CH2 | ||
| C. | C3H7Br→C3H7OH | D. | CH3COOH→CH3COOC2H5 |
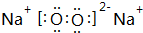 ,含有的化学键类型有离子键、共价键
,含有的化学键类型有离子键、共价键 ,名称是环己烷.
,名称是环己烷.