题目内容
下列对Na2O2的叙述中,正确的是( )
| A、Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物 |
| B、Na2O2中氧元素的化合价为-2价 |
| C、Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2 |
| D、Na2O2需要密封保存 |
考点:钠的重要化合物
专题:元素及其化合物
分析:Na2O2和Na2O都含有钠元素,焰色反应为黄色,其中Na2O2具有强氧化性,可与水、二氧化碳反应生成氧气,Na2O为碱性氧化物,与水反应生成NaOH,以此解答该题.
解答:
解:A.Na2O2能和水反应生成氢氧化钠和氧气,为过氧化物,不是碱性氧化物,故A错误;
B.Na2O2中氧元素的化合价为-1价,故B错误;
C.Na2O与CO2发生化合生成Na2CO3,Na2O2与CO2发生氧化还原反应生成O2,不符合置换反应的定义,故C错误;
D.过氧化钠易与空气中水、二氧化碳反应而变质,应密闭保存,故D正确.
故选D.
B.Na2O2中氧元素的化合价为-1价,故B错误;
C.Na2O与CO2发生化合生成Na2CO3,Na2O2与CO2发生氧化还原反应生成O2,不符合置换反应的定义,故C错误;
D.过氧化钠易与空气中水、二氧化碳反应而变质,应密闭保存,故D正确.
故选D.
点评:本题考查钠的重要化合物知识,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握过氧化钠与水、二氧化碳反应的特点,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
在反应:H2S+H2SO4(浓)═S+SO2+2H2O中,下列说法正确的是( )
| A、S是还原产物,SO2是氧化产物 |
| B、S是氧化产物,SO2是还原产物 |
| C、该反应的电子转移数目是6e- |
| D、H2S是还原剂,被还原为S |
下列说法不正确的是( )
| A、金属氧化物都是碱性氧化物 |
| B、盐电离出的离子一定有金属离子 |
| C、由同种元素组成的物质一定是单质 |
| D、非金属氧化物都是酸性氧化物 |
下列离子方程式中,正确的是( )
| A、石灰石与醋酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、氧化铁和稀硫酸反应:O2-+2H+=H2O |
| C、向NaHSO4溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、向NaHCO3溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++CO32-=BaCO3↓+H2O |
下列有关物质的性质或应用的说法中正确的是( )
| A、Si是一种非金属主族元素,其氧化物可用于制作计算机芯片 |
| B、石油的催化裂化及裂解可以得到较多的轻质油和气态烯烃 |
| C、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物 |
| D、蛋白质溶液中加入浓的硫酸钠溶液,有沉淀析出,这种作用称为变性 |
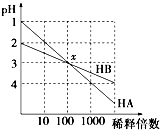 HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )
HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )| A、HA是一种强酸 |
| B、x点,[A-]=[B-] |
| C、HB是一种弱酸 |
| D、原溶液中HA的物质的量浓度为HB的10倍 |
下列关于电解质溶液的叙述正确的是( )
| A、热的纯碱溶液和冷的纯碱溶液洗涤油污效果一样好 |
| B、常温下,将氨水加入到盐酸中,所得溶液中一定存在:c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
| C、中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D、强电解质的水溶液的导电性一定比弱电解质的水溶液强 |