题目内容
10.下列化工生产过程中所发生的主要化学反应不属于氧化还原反应的是( )| A. | 用氯气和消石灰制漂白粉 | B. | 铝热法冶炼金属钒 | ||
| C. | 用石灰石、纯碱、二氧化硅制玻璃 | D. | 电解饱和食盐水制烧碱 |
分析 含元素的化合价变化,为氧化还原反应;不存在元素的化合价变化的反应,不属于氧化还原反应,以此来解答.
解答 解:A.用氯气和消石灰制漂白粉中,Cl元素的化合价既升高又降低,为氧化还原反应,故A不选;
B.铝热法冶炼金属钒,Al元素的化合价升高,V元素的化合价降低,为氧化还原反应,故B不选;
C.用石灰石、纯碱、二氧化硅制玻璃,没有元素的化合价变化,不属于氧化还原反应,故C选;
D.电解饱和食盐水制烧碱,Cl元素的化合价升高,H元素的化合价降低,为氧化还原反应,故D不选;
故选C.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应判断的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列各组混合物中,不能通过分液的方法进行分离的是( )
| A. | 酒精和水 | B. | 植物油和水 | C. | 汽油和水 | D. | 四氯化碳和水 |
18.将5mol/L MgCl2溶液a mL稀释至b mL,稀释后溶液中Cl-的物质的量浓度为( )
| A. | $\frac{5a}{b}$ mol/L | B. | $\frac{10a}{b}$ mol/L | C. | $\frac{b}{5a}$ mol/L | D. | $\frac{a}{b}$ mol/L |
5.某恒温密闭容器中,可逆反应A(s)?B+C(g)-Q达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )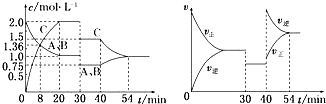

| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内n(A)消耗:n(C)消耗=1:1 | |
| C. | 保持体积不变,向平衡体系中加入A,平衡向正反应方向移动 | |
| D. | 若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q |
15.在无色透明的强酸性溶液中,能大量共存的离子组是( )
| A. | Na+、Mg2+、MnO4-、SO42- | B. | NH4+、Al3+、NO3-、Cl- | ||
| C. | K+、Na+、AlO2-、NO3- | D. | Mg2+、K+、HCO3-、OH- |
20.下列叙述正确的是( )
| A. | 高温下二氧化硅与碳酸钠反应放出二氧化碳,说明硅酸(H2SiO3)的酸性比碳酸强 | |
| B. | 陶瓷、玻璃、水泥容器都能贮存氢氟酸 | |
| C. | 石灰抹墙、水泥砌墙的硬化过程原理不相同 | |
| D. | 硫酸钠溶液、烧碱溶液、硝酸溶液、浓硫酸四种溶液均能用带玻璃塞的试剂瓶保存 |
 .
.