题目内容
18.将5mol/L MgCl2溶液a mL稀释至b mL,稀释后溶液中Cl-的物质的量浓度为( )| A. | $\frac{5a}{b}$ mol/L | B. | $\frac{10a}{b}$ mol/L | C. | $\frac{b}{5a}$ mol/L | D. | $\frac{a}{b}$ mol/L |
分析 根据氯化镁的化学式可知氯离子浓度,然后根据稀释过程中溶质的物质的量不变计算出稀释后溶液中氯离子的物质的量浓度.
解答 解:5mol/L MgCl2溶液中氯离子的浓度为:5mol/L×2=10mol/L,
将amL稀释至bmL,稀释过程中氯离子的物质的量不变,则稀释后溶液中氯离子浓度为:$\frac{10mol/L×a×1{0}^{-3}L}{b×1{0}^{-3}L}$=$\frac{10a}{b}$mol/L,
故选B.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式即可解答,注意掌握溶液稀释过程中溶质的物质的量不变,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
8.下列说法中正确的是( )
| A. | 2mol水的摩尔质量是1mol 水的摩尔质量的2倍 | |
| B. | 阿伏伽德罗常数就是6.02×1023 | |
| C. | 6.02×1023 mol-1叫做阿伏伽德罗常数 | |
| D. | 科学上规定含6.02×1023个粒子的任何粒子集合体计量为1mol |
9.高温下,硫酸亚铁发生如下反应:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
| A. | BaSO4 | B. | BaS | C. | BaSO3 | D. | BaSO3和BaSO4 |
6.氯气是有毒气体,曾被德国法西斯制成毒气弹用于侵略战争.当这种毒气顺风扩散时,通常可选用的防护办法是( )
①人躲到低洼的地方去;
②人躲到较高的地方去;
③多饮豆浆和牛奶;
④用沾有碳酸钠溶液的软布蒙面.
①人躲到低洼的地方去;
②人躲到较高的地方去;
③多饮豆浆和牛奶;
④用沾有碳酸钠溶液的软布蒙面.
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ②③④ |
13.下列各项正确的是( )
| A. | 钠与水反应的离子方程式:Na+H2O═Na++OH-+H2↑ | |
| B. | 铁与水蒸气反应的化学方程式:3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2 | |
| C. | 镁、铝与沸水不可能反应 | |
| D. | 钠和硫酸铜溶液反应的离子方程式:2Na+Cu2+═2Na++Cu |
10.下列化工生产过程中所发生的主要化学反应不属于氧化还原反应的是( )
| A. | 用氯气和消石灰制漂白粉 | B. | 铝热法冶炼金属钒 | ||
| C. | 用石灰石、纯碱、二氧化硅制玻璃 | D. | 电解饱和食盐水制烧碱 |
7.构成物质的聚集状态有固、液、气三种状态,科学研究表明,除了上述三种状态之外,还存在一些其它聚集状态,下列物质的状态属于其它聚集状态的是( )
①非晶体;②液晶;③纳米材料;④等离子体.
①非晶体;②液晶;③纳米材料;④等离子体.
| A. | ① | B. | ①② | C. | ①②③ | D. | ①②③④ |
8.313K时,水的Kw=3.0×10-14,则在313K时,c(H+)=10-7 mol/L的溶液( )
| A. | 呈酸性 | B. | 呈中性 | C. | 呈碱性 | D. | 无法判断 |
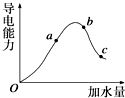 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答: