题目内容
某阳离子与Ar具有相同的电子层结构,阴离子与Ne具有相同的电子层结构,该阴、阳离子所形成的化合物可能是( )
| A、K2S |
| B、NaF |
| C、CaF2 |
| D、Na2O |
考点:原子结构与元素的性质
专题:原子组成与结构专题
分析:某阳离子与Ar具有相同的电子层结构,则该阳离子元素位于第四周期,阴离子与Ne具有相同的电子层结构,则该阴离子元素位于第二周期,据此分析解答.
解答:
解:某阳离子与Ar具有相同的电子层结构,则该阳离子元素位于第四周期,阴离子与Ne具有相同的电子层结构,则该阴离子元素位于第二周期,
A.S元素位于第三周期,不符合,故A错误;
B.Na元素位于第三周期,不符合,故B错误;
C.Ca元素位于第四周期、F元素位于第二周期,符合题意,故C正确;
D.Na元素位于第三周期,不符合,故D错误;
故选C.
A.S元素位于第三周期,不符合,故A错误;
B.Na元素位于第三周期,不符合,故B错误;
C.Ca元素位于第四周期、F元素位于第二周期,符合题意,故C正确;
D.Na元素位于第三周期,不符合,故D错误;
故选C.
点评:本题考查了原子结构和元素性质,阴阳离子电子层结构对应的稀有气体元素结合原子结构分析解答,题目难度不大.

练习册系列答案
相关题目
下列物质可以发生加成反应的是( )
| A、乙烷 | B、环丙烷 |
| C、乙烯 | D、聚乙烯 |
下列各组物质在溶液中反应时,以任意比例混合均能用同一离子方程式表示的是( )
| A、AgNO3溶液和稀氨水 |
| B、Na2S和盐酸 |
| C、AlCl3溶液和氨水 |
| D、Fe和稀硝酸 |
下列反应中,属于加成反应的是( )
| A、乙烯通入酸性KMnO4溶液 |
| B、乙烷与溴蒸气反应 |
| C、乙烯在一定条件下与水反应生成乙醇 |
| D、乙烯燃烧生成二氧化碳和水 |
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )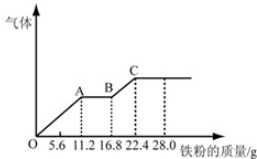

| A、原混合酸中NO3-的物质的量为0.4mol |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为4mol?L-1 |
下列说法正确的是( )
| A、变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 |
| B、因为NaCl的水溶液能导电,所以NaCl溶液属于强电解质 |
| C、铝合金的大量使用是因为人们能用焦炭等还原剂从氧化铝中获取铝 |
| D、37Cl 是氯元素的一种核素,37Cl的中子数和电子数之差是3 |
在下列给定条件的溶液中,一定能大量共存的粒子组是( )
| A、能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- | ||
B、常温下,
| ||
| C、水电离的c(H+)水=1.0×10-13mol?L-1溶液中:AlO2-、K+、SO42-、Br- | ||
| D、与铝反应产生大量氢气的溶液:Na+、K+、NH4+、NO3- |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、常温常压下,4g CH4含NA个共价键 |
| B、常温常压下,22.4L氦气含有的原子数为2NA |
| C、1mol S在足量O2中燃烧,转移的电子数为6NA |
| D、0.1mol?L-1的碳酸氢钠溶液中含钠离子数为0.1NA |