题目内容
下列离子方程式正确的是( )
| A、碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、Fe3O4溶液稀盐酸:Fe3O4+8H+═3Fe3++4H2O |
| C、用烧碱溶液吸收氯气:Cl2+2OH-═Cl-+ClO-+H2O |
| D、向硫酸亚铁溶液中加入用硫酸酸化的H2O2溶液Fe2++H2O2+2H+═Fe3++4H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.醋酸为弱电解质,离子方程式中应该保留分子式;
B.四氧化三铁与稀盐酸反应生成铁离子和亚铁离子,离子方程式两边电荷不守恒;
C.氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
D.根据电荷守恒判断,该离子方程式两边电荷不守恒.
B.四氧化三铁与稀盐酸反应生成铁离子和亚铁离子,离子方程式两边电荷不守恒;
C.氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
D.根据电荷守恒判断,该离子方程式两边电荷不守恒.
解答:
解:A.碳酸钙溶于醋酸,碳酸钙和醋酸都不能拆开,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故A错误;
B.Fe3O4溶液稀盐酸,反应生成亚铁离子和铁离子,正确的离子方程式为:Fe3O4+8H+═2Fe3++Fe2++4H2O,故B错误;
C.烧碱溶液吸收氯气,反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故C正确;
D.硫酸亚铁溶液中加入用硫酸酸化的H2O2溶液,反应生成铁离子和水,离子方程式必须遵循电荷守恒,正确的离子方程式为:2Fe2++H2O2+2H+═2Fe3++4H2O,故D错误;
故选C.
B.Fe3O4溶液稀盐酸,反应生成亚铁离子和铁离子,正确的离子方程式为:Fe3O4+8H+═2Fe3++Fe2++4H2O,故B错误;
C.烧碱溶液吸收氯气,反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故C正确;
D.硫酸亚铁溶液中加入用硫酸酸化的H2O2溶液,反应生成铁离子和水,离子方程式必须遵循电荷守恒,正确的离子方程式为:2Fe2++H2O2+2H+═2Fe3++4H2O,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
硅是带来人类文明的重要元素之一,下列有关说法错误的是( )
| A、水泥、陶瓷、玻璃是三大重要的硅酸盐产品 |
| B、水玻璃是建筑行业经常使用的一种黏合剂 |
| C、刚玉、水晶、石英的主要成分是二氧化硅 |
| D、晶体硅是一种重要的半导体材料 |
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )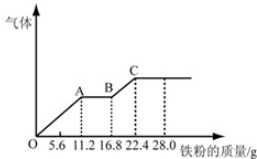

| A、原混合酸中NO3-的物质的量为0.4mol |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为4mol?L-1 |
在下列给定条件的溶液中,一定能大量共存的粒子组是( )
| A、能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- | ||
B、常温下,
| ||
| C、水电离的c(H+)水=1.0×10-13mol?L-1溶液中:AlO2-、K+、SO42-、Br- | ||
| D、与铝反应产生大量氢气的溶液:Na+、K+、NH4+、NO3- |
下列离子方程式正确的是( )
| A、在硫酸铜溶液中加入过量氢氧化钡溶液:Ba2++SO42-=BaSO4↓ |
| B、碳酸氢钠溶液与少量石灰水反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
| C、向氯化铝溶液中加入过量氨水:A13++4NH3?H2O=A1O2-+4NH4++2H2O |
| D、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+2H2O |
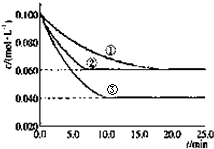 在密闭容器中,反应A(g)+2B(g)?C(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L;c(B)=0.200mol/L;c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.下列说法正确的是( )
在密闭容器中,反应A(g)+2B(g)?C(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L;c(B)=0.200mol/L;c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.下列说法正确的是( )| A、实验②平衡时B的转化率为60% |
| B、反应A(g)+2B(g)?C(g)的△H>0 |
| C、若反应①、②的平衡常数分别为K1、K2,则K1<K2 |
| D、减小反应③的压强,可以使平衡时c(A)=0.060mol/L |