题目内容
【题目】下列用电子式表示化合物的形成过程正确的是( )
A.![]()
B.![]()
C.![]()
D.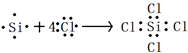
【答案】C
【解析】解:A.二氧化碳是氧原子和碳原子之间通过共价键形成的共价化合物,形成过程为: ![]() ,故A错误;B.硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为:
,故A错误;B.硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为: ![]() ,故B错误;
,故B错误;
C.H2O为共价化合物,各原子达到稳定结构,用电子式表示形成过程为 ![]() ,故C正确;
,故C正确;
D.四氯化硅中所有原子最外层都满足8电子稳定结构;用电子式表示四氯化硅的形成过程为: 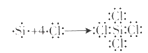 ,故D错误;
,故D错误;
故选:C.
A.二氧化碳是氧原子和碳原子之间通过共价键形成的共价化合物,存在C=O;
B.硫化钠为离子化合物,2个钠离子不能合写;
C.水为共价化合物,氧原子与两根氢原子分别共用1对电子;
D.四氯化硅中氯原子最外层有8个电子.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
【题目】从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O.
(1)为了加快反应速率,不可以采取的措施有(填序号,下同). A.使用催化剂 B.提高氧气的浓度
C.提高反应的温度 D.降低反应的温度
(2)已知该反应为放热反应,如图能正确表示该反应中能量变化的是 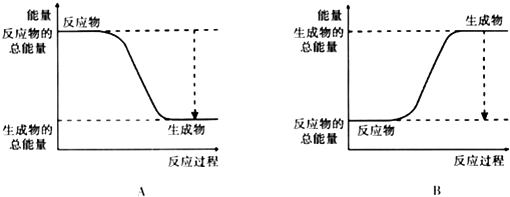
(3)从断键和成键的角度分析上述反应中能量的变化.已知化学键的键能如表:
化学键 | H﹣H | O=O | H﹣O |
键能kJmol﹣1 | 436 | 496 | 463 |
由此计算2mol H2在氧气中燃烧生成气态水放出的热量 .