题目内容
【题目】分析、归纳、探究是学习化学的重要方法和手段之一。下面就电解质A回答有关问题(假定以下都是室温时的溶液)。
(1)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=a。
①试说明HnB的酸性强弱____。
②当a=10时,A溶液呈碱性的原因是(用离子方程式表示)______。
③当a=10、n=1时,A溶液中各种离子浓度由大到小的顺序为____,(OH-)-c(HB)=______。
④当n=1、c=0.1、溶液中c(HB):c(B-)=1∶99时,A溶液的pH为___(保留整数值)。
(2)已知难溶电解质A的化学式为XnYm,相对分子质量为M,测得其饱和溶液的密度为ρg/cm3,Xm+离子的浓度为c mol/L,则该难溶物XnYm的溶度积常数为Ksp=___。
【答案】当a=7时,HnB为强酸,当a>7时,HnB为弱酸 Bn-+H2O![]() HB(n-1)-+OH- c(Na+)> c(Bn-)> c(OH-)> c(H+) 10-10mol/L 11 (m/n)mcm+n
HB(n-1)-+OH- c(Na+)> c(Bn-)> c(OH-)> c(H+) 10-10mol/L 11 (m/n)mcm+n
【解析】
(1)①依据盐溶液pH分析判断对应酸碱的强弱,弱离子水解盐溶液显示了酸碱性;
②依据盐类水解的实质分析书写离子方程式;
③根据溶液中的pH、电荷守恒、物料守恒、盐的水解原理进行分析、计算、比较离子浓度大小;
④根据c(HB):c(B-)=1:99计算出水解生成氢氧根离子的浓度,再根据水的离子积计算出溶液中氢离子的浓度,然后计算pH;
(2)根据电解质A的化学式写出溶解平衡,根据溶度积常数表达式及题数中数据 计算出该难溶物XnYm的溶度积常数为Ksp。
(1)①电解质A的化学式为NanB,测得浓度为cmol·L-1的A溶液的pH=a.当a=7说明是强酸强碱盐,HnB为强酸,当a大于7,NanB为强碱弱酸盐,在溶液中发生了水解:Bn-+H2O![]() HB(n-1)-+OH-,HnB为弱酸;
HB(n-1)-+OH-,HnB为弱酸;
②NanB溶液的pH=10,NanB为强碱弱酸盐,在溶液中发生了水解:Bn-+H2O![]() HB(n-1)-+OH-;
HB(n-1)-+OH-;
③当a=10,n=1时,由于B-离子水解,溶液呈碱性,溶液中B-离子浓度减小,小于溶液中钠离子的浓度,水解是少量的,所以A溶液中各种离子浓度由大到小的顺序为:c(Na+)>c(B-)>c(OH-)>c(H+)。溶液中存在电荷守恒:c(B-)+c(OH-)=c(H+)+c(Na+);物料守恒:c(Na+)=c(HB)+c(B-);将钠离子浓度带入电荷守恒可得:c(B-)+c(OH-)=c(H+)+c(HB)+c(B-),c(OH-)-c(HB)=c(H+)=1×10-10mol·L-1;
③当n=1、c=0.1,溶液中c(HB):c(B-)=1:99时,参与水解的B-离子为1%,水解生成OH-浓度为:0.1mol·L-1×1%=0.001mol·L-1,则![]() ,所以溶液的pH为11;
,所以溶液的pH为11;
(2)已知难溶电解质A的化学式为XnYm,相对分子质量为M,测得其饱和溶液的密度为ρg·cm-3,Xm+离子的浓度为cmol·L-1,XnYm的溶解平衡为:XnYm(s)![]() nXm+(aq)+mYn-(aq)),Xm+离子的浓度为cmol·L-1,Yn-的浓度为
nXm+(aq)+mYn-(aq)),Xm+离子的浓度为cmol·L-1,Yn-的浓度为![]() mol·L-1,
mol·L-1,![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,不溶于水,易溶于醇等有机溶剂。实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
已知:①乙醇在浓硫酸存在下在140℃脱水生成乙醚
2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
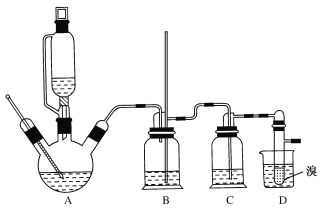
②实验中常因温度过高而使乙醇和浓硫酸反应生成少量SO2和CO2,用12.0g溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示:
有关数据列表如下:
类别 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是___。要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___。
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是____。
(3)在装置C中应加入NaOH溶液,其目的是____。
(4)装置D中小试管内盛有液溴,判断该制备反应已经结束的最简单方法是___。
(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___层(填“上”或“下”)。若产物中有少量未反应的Br2,最好用___洗涤除去;若产物中有少量副产物乙醚,可用____(填操作方法名称)的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是___。
(7)若实验结束后得到9.4g产品,1,2—二溴乙烷的产率为___。