��Ŀ����
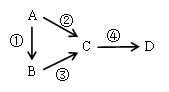
A��B��C��D��E��FΪ��ѧ��ѧ�еij������ʣ�������A��1~2�ֶ�����Ԫ����ɣ���һ��������������ת����ϵ���������������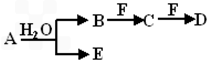
��1����������AΪ��ɫ����
����F��һ�ֽ������ʣ���д��B������F��Ӧ����C������E�����ӷ���ʽ��_________________ _____________��
����CΪֱ���ͷ��ӣ�E����Ư���ԣ�����F��ɫ��Ӧ�ʻ�ɫ����д����ҵ���Ʊ�����F�Ļ�ѧ��Ӧ����ʽ��_______ ____________��__________ _____��
��2����AΪ����ɫ���壬��A���ʵĵ���ʽΪ��_________________��
��������B��D����Է���������ȣ�����C�Ĵ����ŷ�������������صĻ������⼴_____ _____��
��������A��D����Է����������,�������ӷ���ʽ��ʾ����F��ˮ��Һ�����Ե�ԭ��_____ _____��
��3)������A��һ��Ԫ��ԭ�ӵ�����������Ϊ�ڲ����������1/5����B��D�ֱ�����ˮ��������Һ��ǡ��������ϣ��ɵ�һ��������Ԫ�ص�����Һ����д��A�Ļ�ѧʽ________��
��1����Fe+4H++NO3- =Fe3++NO+2H2O
��CO2+NH3+NaCl+H2O=NaHCO3��+NH4Cl 2NaHCO3=Na2CO3+H2O+CO2��
��2��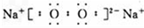
��������Al3+ + 3H2O? Al(OH)3 + 3H+��3��Mg3N2
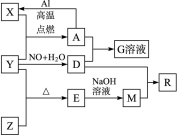
���������������1��������A��1~2�ֶ�����Ԫ�������AΪ��ɫ���壬��A��ˮ��Ӧ���ɵ������ܺͽ�����Ӧ����AΪNO2������B������F��Ӧ����C������E�����ӷ���ʽΪ��Fe+4H++NO3- =Fe3++NO+2H2O����CΪֱ���ͷ���ΪCO2��E����Ư����Ϊ�����ᣬ����F��ɫ��Ӧ�ʻ�ɫ��FΪ̼���ƣ���ҵ���Ʊ�̼���Ƶķ�Ӧ����ʽΪ��CO2+NH3+NaCl+H2O=NaHCO3��+NH4Cl 2NaHCO3=Na2CO3+H2O+CO2������2������ɫ����Ϊ�������ƣ��������Ƶĵ���ʽΪ��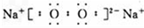 ��������B��D����Է���������ȣ�����C�Ĵ����ŷ�������������صĻ������⣬��BΪ������FΪ���⣬CΪ��������DΪ��������������صĻ������⼴�γ����ꣻ��������A��D����Է���������ȣ���DΪAl(OH)3����F��ˮ��Һ�����Ե�ԭ��Ϊ��Al3+ + 3H2O? Al(OH)3 + 3H+����3������A��һ��Ԫ��ԭ�ӵ�����������Ϊ�ڲ����������1/5����B��D�ֱ�����ˮ��������Һ��ǡ��������ϣ��ɵ�һ��������Ԫ�ص�����Һ��AΪ��Mg3N2��
��������B��D����Է���������ȣ�����C�Ĵ����ŷ�������������صĻ������⣬��BΪ������FΪ���⣬CΪ��������DΪ��������������صĻ������⼴�γ����ꣻ��������A��D����Է���������ȣ���DΪAl(OH)3����F��ˮ��Һ�����Ե�ԭ��Ϊ��Al3+ + 3H2O? Al(OH)3 + 3H+����3������A��һ��Ԫ��ԭ�ӵ�����������Ϊ�ڲ����������1/5����B��D�ֱ�����ˮ��������Һ��ǡ��������ϣ��ɵ�һ��������Ԫ�ص�����Һ��AΪ��Mg3N2��
���㣺���ƶ�

���з�Ӧ�У���Ӧ������������ص���
| A������ͨ�����ȵ�CuO��ĩ | B��������̼ͨ��Na2O2��ĩ |
| C������Fe2O3�������ȷ�Ӧ | D����п��Ͷ��Cu(NO3)2��Һ |


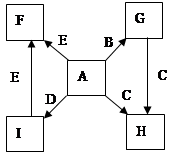



 Ti
Ti