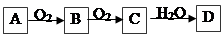题目内容
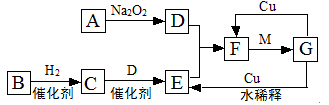
A、B、C、D、E、F、G七种元素均是短周期元素,且原子序数依次增大。A原子无中子, B、G原子的最外层电子数均为其电子层数的两倍,D、G元素原子的最外层电子数相等。X、Y、Z、W、甲、乙六种物质均由上述元素的两种或三种元素组成,元素B形成的单质M与甲、乙(甲、乙是高中常见的浓酸)均能反应(相对分子质量甲< 乙)转化关系如图(反应条件略去),原子E最外层电子数和其电子层数相等。元素F形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料。请回答下列问题:
(1)A2D的熔沸点比A2G高的原因是 。B、D、G各一个原子构成每原子均满足8电子的分子,其电子式是 。
(2)E4B3和水反应的化学方程式 。
(3)写出M与甲的浓溶液加热时反应的化学方程式 。
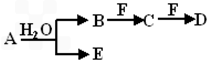
(4)X、Y、Z、W属于同一类物质,这类化合物固态时的晶体类型为 ;X、Y、W都能与Z反应,则Z的结构式为 。
(5)已知CH4 (g)+ 2O2(g)=CO2 (g)+2H2O(l) △H1=a kJ/mol
欲计算反应CH4 (g)+ 4NO (g)=2N2 (g)+CO2 (g)+2H2O(l)的焓变△H2 ,则还需要查找某化合反应的焓变△H3,当反应中各物质化学计量数之比为最简整数比时 △H3 =" b" kJ/mol,则该反应的热化学方程式为 。
据此计算出△H2 = kJ/mol(用含a和b的式子表示)。
(1)水分子间存在氢键(2分) 电子式省(2分)
(2)Al4C3+6H2O=4Al(OH)3↓+3CH4↑(2分)
(3)C + 4HNO3(浓) CO2↑+ 4NO2↑+ 2H2O (2分)
CO2↑+ 4NO2↑+ 2H2O (2分)
(4)分子晶体 (1分) H—O—H(1分)
(5)N2(g) + O2(g)=2NO(g) △H3 =" b" kJ/mol (2分) a - 2b(2分)
解析试题分析: A原子无中子,可知A为H;B、G原子的最外层电子数均为其电子层数的两倍,可知B为C,G为S;D、G元素原子的最外层电子数相等,可知D为O;那么C一定为N;原子E最外层电子数和其电子层数相等,可知E为Al;元素F形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料,可知F为Si;相对分子质量甲< 乙,可知甲为HNO3,乙为H2SO4;X为NO2;W为SO2;Y为CO2;Z为H2O;
考点:考查