题目内容
2.CoCl2•6H2O是一种饲料营养强化剂.以含钴单质废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种新工艺流程如图: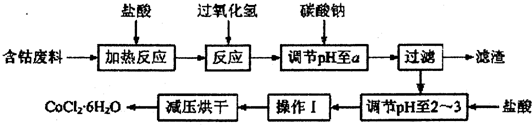
已知:
①CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
(1)钴与盐酸反应的化学方程式为Co+2HCl=CoCl2+H2↑.
(2)流程中加入碳酸钠调节pH至a,a的范围是5.2~7.6;滤渣中含有的Al(OH)3是良好的阻燃剂,其原理是Al(OH)3受热分解时吸收大量的热,使环境温度下降;同时生成的耐高温、稳定性好的Al2O3覆盖在可燃物表面,阻燃效果更佳;加盐酸调节pH至2~3的目的是抑制Co2+的水解,防止在后续的操作中形成Co(OH)2杂质.
(3)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(4)制得的CoCl2•6H2O需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定产品中CoCl2•6H2O含量,某同学将119g样品溶于水形成100ml溶液,取25mL于烧杯中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称得质量为28.7g,计算产品中CoCl2•6H2O含量为80%.(已知:CoCl2•6H2O化学式量为238,AgCl为143.5,假设杂质不与AgNO3溶液反应,结果保留两位有效数字)
分析 (1)钴与盐酸反应生成氯化钴和氢气;
(2)调节溶液的PH值,使溶液中铁离子和铝离子生成沉淀,而钴离子存在溶液中,从而将铁离子、铝离子和钴离子分开;
(3)根据从溶液中制取固体的方法制取氯化钴固体,从而确定操作步骤;
(4)温度高时,CoCl2•6H2O分解;
(5)根据CoCl2•6H2O与AgCl的关系式求质量分数.
解答 解:(1)钴与盐酸反应生成氯化钴和氢气,反应的化学方程式为Co+2HCl=CoCl2+H2↑,
故答案为:Co+2HCl=CoCl2+H2↑;
(2)废料加入盐酸后生成氯化物,然后加入双氧水,二价铁离子被双氧水氧化生成三价铁离子,根据沉淀的PH值表格知,当溶液的PH值为5.2时,铁离子和铝离子被完全沉淀,当溶液的PH值为7.6时,钴离子才开始产生沉淀,所以要想将铁离子、铝离子和钴离子分离,溶液的pH值应该不小于5.2不大于7.6,;Al(OH)3受热分解时吸收大量的热,使环境温度下降;同时生成的耐高温、稳定性好的Al2O3覆盖在可燃物表面,进行阻燃;加盐酸调节pH至2~3,可以防止钴离子水解
故答案为:5.2~7.6;Al(OH)3受热分解时吸收大量的热,使环境温度下降;同时生成的耐高温、稳定性好的Al2O3覆盖在可燃物表面,阻燃效果更佳;抑制Co2+的水解,防止在后续的操作中形成Co(OH)2杂质;
(3)从溶液中制取固体的方法制取氯化钴固体,其操作步骤是蒸发浓缩、冷却结晶和过滤,故答案为:蒸发浓缩、冷却结晶;
(4)根据题意知,CoCl2•6H2O常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴,为防止其分解,制得的CoCl2•6H2O需减压烘干;故答案为:降低烘干温度,防止产品分解;
(5)根据CoCl2•6H2O~2AgCl,
238 287
x 28.7g,x=23.8g,
则粗产品中CoCl2•6H2O的质量分数是$\frac{23.8g×\frac{100mL}{25mL}}{119g}$×100%=80%,
故答案为:80%
点评 本题考查了实验方案设计中的有关知识,难度较大,比较突出的难点是:1、误差的分析不知如何寻找“题眼”;2、信息题中信息的阅读、提取有用信息然后进行加工的方法不会,从而导致做题错误较多.

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案| A. | 等于50 mL | B. | 大于50 mL | C. | 等于100 mL | D. | 大于100 mL |
| A. | 用电子式表示溴化氢的形成过程为: | |
| B. | 海水中Br-的电子式为: | |
| C. | 海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl | |
| D. | 氯离子的结构示意图为: |
| A. | 丙烷与氯气在光照的作用下的反应 | B. | 乙烯与溴的四氯化溶液的反应 | ||
| C. | 乙烯与水的反应 | D. | 乙烯自身生成聚乙烯的反应 |
| A. | 淀粉、纤维素、蛋白质在一定条件下均能发生水解反应,水解产物不相同 | |
| B. | 汽油、油脂不一定能使酸性高锰酸钾溶液褪色 | |
| C. | 煤的干馏、石油催化重整、石油裂化、煤的液化都属于化学变化 | |
| D. | 甘氨酸和谷氨酸在一定条件下最多能形成三种二肽 |
| A. | 钢铁在弱碱性条件下发生电化学腐蚀的正极反应是:O2+2H2O+4e-═4OH- | |
| B. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 | |
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| D. | 当镀锌铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
①苯 ②苯酚 ③甲苯 ④乙醇 ⑤己烯 ⑥己烷 ⑦亚硫酸.
| A. | ②③⑤⑥ | B. | ②④⑥⑦ | C. | ②⑤⑦ | D. | 全部 |
 如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )
如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )| A. | 三种元素的原子半径的大小顺序是B<A<C | |
| B. | A元素最高价氧化物对应水化物具有强氧化性和不稳定性 | |
| C. | B元素的氧化物和氢化物的水溶液都呈酸性 | |
| D. | C元素的单质是非金属单质中唯一能跟水激烈反应的单质 |

 ,它的单质能(填能或不能)与氢氧化钠溶液反应.
,它的单质能(填能或不能)与氢氧化钠溶液反应.