题目内容
【题目】已知H2、CO、CH4的燃烧热分别为ΔH1=-285.8 kJ/mol、ΔH2=-283 kJ/mol、ΔH3=-890 kJ/mol。H2O(g)=H2O(l) ΔH4=-44 kJ/mol。回答下列问题:
(1)用CH4替代水煤气作家用燃气的优点是____________________。将煤气灶改为天然气灶时,应适当调_________(填“大”或“小”)空气进气阀门。
(2)合成氨厂一般采用烃(以CH4为例)和水蒸气反应制取原料气H2,发生如下反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
①该反应的ΔH=________________。
②当该反应达到平衡状态时,下列说法一定正确的是__________(填字母)。
A.v(CH4)=v(CO) B.加入催化剂,ΔH不变
C.升高温度,平衡常数K增大 D.CH4与H2O的转化率相等
③T℃时,该反应的初始浓度与起始速率的部分数据如下:
初始浓度/mol·L-1 | 起始速率/mol3·L-3·s-1 | |
c(CH4) | c(H2O) | v |
0.10 | 0.10 | 1.0×10-4 |
0.10 | 0.20 | 4.0×10-4 |
0.30 | 0.20 | 1.2×10-3 |
写出起始速率与初始浓度的关系式[用c(CH4)、c(H2O)及适当的速率常数表示]v=________。
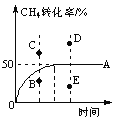
④T℃时,在一个体积可变的恒压密闭容器中,充入0.1 mol CH4、0.1 mol H2O(g)发生反应,起始时容器的体积为1 L。CH4的转化率与反应时间的关系如图中曲线A所示。则T℃时该反应的平衡常数K=____________。若温度与投料方式相同,该反应在容积为1 L的恒容密闭容器中进行,刚达平衡状态的点是__________(选填B、C、D、E)。
【答案】
(1)等体积的燃气放热量多;大
(2)①+206.4 kJ/mol;②ABC;③0.1s-1·c(CH4)·c2(H2O);④0.03;B
【解析】
试题分析:(1) 根据H2、CO、CH4的燃烧热分别为ΔH1=-285.8 kJ/mol、ΔH2=-283 kJ/mol、ΔH3=-890 kJ/mol。有H2(g)+![]() O2(g)=H2O(l)△H=-285.8kJ/mol,CO(g)+
O2(g)=H2O(l)△H=-285.8kJ/mol,CO(g)+![]() O2(g)=CO2(g)△H=-283.0 kJ/mol,CH4(g)+2O2(g)=2H2O(l)+CO2 (g)△H=-890kJ/mol。等体积的CH4燃烧放出的热量比水煤气多,等体积的甲烷燃烧消耗的氧气比水煤气多,将煤气灶改为天然气灶时,应适当调大空气进气阀门,故答案为:等体积的燃气放热量多;大;
O2(g)=CO2(g)△H=-283.0 kJ/mol,CH4(g)+2O2(g)=2H2O(l)+CO2 (g)△H=-890kJ/mol。等体积的CH4燃烧放出的热量比水煤气多,等体积的甲烷燃烧消耗的氧气比水煤气多,将煤气灶改为天然气灶时,应适当调大空气进气阀门,故答案为:等体积的燃气放热量多;大;
(2)①根据H2(g)、CO(g)和CH4(g)的燃烧热分别为285.8kJmol-1、283.0kJmol-1和890kJ/mol,分别写出热化学方程式:
H2(g)+![]() O2(g)=H2O(l)△H=-285.8kJ/mol……①
O2(g)=H2O(l)△H=-285.8kJ/mol……①
CO(g)+![]() O2(g)=CO2(g)△H=-283.0 kJ/mol……②
O2(g)=CO2(g)△H=-283.0 kJ/mol……②
CH4(g)+2O2(g)=2H2O(l)+CO2 (g)△H=-890kJ/mol……③,根据盖斯定律,将③-②-①×3,得:CH4(g)+H2O(l) ![]() CO(g)+3H2(g) △H=-890kJ/mol-(-283.0 kJ/mol)-(-285.8kJ/mol)×3=+250.4 kJ/mol,又H2O(g)=H2O(l) ΔH4=-44 kJ/mol,因此CH4(g)+H2O(g)
CO(g)+3H2(g) △H=-890kJ/mol-(-283.0 kJ/mol)-(-285.8kJ/mol)×3=+250.4 kJ/mol,又H2O(g)=H2O(l) ΔH4=-44 kJ/mol,因此CH4(g)+H2O(g) ![]() CO(g)+3H2(g) △H==+250.4 kJ/mol+(-44 kJ/mol)=+206.4 kJ/mol,故答案为:+206.4 kJ/mol;
CO(g)+3H2(g) △H==+250.4 kJ/mol+(-44 kJ/mol)=+206.4 kJ/mol,故答案为:+206.4 kJ/mol;
②A.根据反应方程式CH4(g)+H2O(g) ![]() CO(g)+3H2(g),v(CH4)=v(CO),故A正确;B.催化剂不改变反应的ΔH,故B正确;C.升高温度,平衡正向移动,平衡常数K增大,故C正确;D.CH4与H2O的转化率与二者的起始量应该,不一定相等,故D错误;故选ABC;
CO(g)+3H2(g),v(CH4)=v(CO),故A正确;B.催化剂不改变反应的ΔH,故B正确;C.升高温度,平衡正向移动,平衡常数K增大,故C正确;D.CH4与H2O的转化率与二者的起始量应该,不一定相等,故D错误;故选ABC;
③根据表格中数据可知,反应速率与c(H2O)的平方成正比,与c(CH4)成正比,v=0.1s-1·c(CH4)·c2(H2O),故答案为:0.1s-1·c(CH4)·c2(H2O);
④ CH4(g)+H2O(g) ![]() CO(g)+3H2(g)
CO(g)+3H2(g)
起始(mol)0.1 0.1 0 0
反应 0.05 0.05 0.05 0.15
平衡 0.05 0.05 0.05 0.15
平衡时气体的物质的量为0.3mol,相同压强下,体积为1.5L
平衡常数K=![]() =
=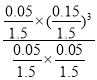 =0.03;该反应属于气体的物质的量增大的反应,平衡时体积大于1L,若温度与投料方式相同,该反应在容积为1 L的恒容密闭容器中进行,相当于增大压强,平衡逆向移动,甲烷的转化率减小,反应速率增大,建立平衡所需的时间减少,故选B,故答案为:0.03;B。
=0.03;该反应属于气体的物质的量增大的反应,平衡时体积大于1L,若温度与投料方式相同,该反应在容积为1 L的恒容密闭容器中进行,相当于增大压强,平衡逆向移动,甲烷的转化率减小,反应速率增大,建立平衡所需的时间减少,故选B,故答案为:0.03;B。