题目内容
【题目】2014年我国的冶金行业深受经济危机的冲击,尤其是Al、Fe的价格下滑幅度很大。请完成下面问题:
(1)冶炼后的铝渣中含有大量的硅酸铝钙(Al2Ca2Si5O15),可作耐火纤维的原料。硅酸铝钙用氧化物形式表示为______________________。
(2) 由下列物质冶炼相应金属时采用电解法的是 。
a. Fe2O3 b. NaCl c. Cu2S d. Al2O3
(3)高铁电池具有容量高、安全性能好和价格低廉等特点,如图是高铁电池的实验装置。

已知:放电后两极得到相同价态铁的化合物。
①电池放电时正极发生的电极反应式是______________________。
②若该电池属于二次电池,则充电时阴极的电极反应式为_______________________。
③已知盐桥中含有饱和KCl溶液,放电时,盐桥的作用是_________________。
【答案】
(1)2CaO·Al2O3·5SiO2;(2)bd
(3)①FeO42-+3e-+4H2O=Fe(OH)3+5OH-;②Fe(OH)3+3e-=Fe+3OH-
③形成闭合回路,并保持两边溶液呈电中性
【解析】
试题分析:(1)硅酸铝钙(Al2Ca2Si5O15),用氧化物形式表示为2CaO·Al2O3·5SiO2,故答案为:2CaO·Al2O3·5SiO2;
(2) 在金属活动性顺序表中位于铝前面的金属冶炼时一般采用电解法,故选bd;
(3) ①FeO42-在正极得电子生成Fe3+,生成其电极反应式为:FeO42-+4H2O+3e-═Fe(OH)3↓+5OH-;故答案为:FeO42-+4H2O+3e-═Fe(OH)3↓+5OH-;
②充电时Fe(OH)3在阴极得电子生成Fe,其电极反应式为:Fe(OH)3+3e-═Fe+3OH-,故答案为:Fe(OH)3+3e-═Fe+3OH-;
③盐桥中含有饱和KCl溶液,盐桥能够使装置形成闭合回路,并保持两边溶液呈电中性,故答案为:形成闭合回路,并保持两边溶液呈电中性。

【题目】已知H2、CO、CH4的燃烧热分别为ΔH1=-285.8 kJ/mol、ΔH2=-283 kJ/mol、ΔH3=-890 kJ/mol。H2O(g)=H2O(l) ΔH4=-44 kJ/mol。回答下列问题:
(1)用CH4替代水煤气作家用燃气的优点是____________________。将煤气灶改为天然气灶时,应适当调_________(填“大”或“小”)空气进气阀门。
(2)合成氨厂一般采用烃(以CH4为例)和水蒸气反应制取原料气H2,发生如下反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
①该反应的ΔH=________________。
②当该反应达到平衡状态时,下列说法一定正确的是__________(填字母)。
A.v(CH4)=v(CO) B.加入催化剂,ΔH不变
C.升高温度,平衡常数K增大 D.CH4与H2O的转化率相等
③T℃时,该反应的初始浓度与起始速率的部分数据如下:
初始浓度/mol·L-1 | 起始速率/mol3·L-3·s-1 | |
c(CH4) | c(H2O) | v |
0.10 | 0.10 | 1.0×10-4 |
0.10 | 0.20 | 4.0×10-4 |
0.30 | 0.20 | 1.2×10-3 |
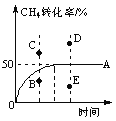
写出起始速率与初始浓度的关系式[用c(CH4)、c(H2O)及适当的速率常数表示]v=________。
④T℃时,在一个体积可变的恒压密闭容器中,充入0.1 mol CH4、0.1 mol H2O(g)发生反应,起始时容器的体积为1 L。CH4的转化率与反应时间的关系如图中曲线A所示。则T℃时该反应的平衡常数K=____________。若温度与投料方式相同,该反应在容积为1 L的恒容密闭容器中进行,刚达平衡状态的点是__________(选填B、C、D、E)。