题目内容
8.在用海带提取碘的实验中,进行萃取和分液操作时要用到的仪器是( )| A. | 分液漏斗 | B. | 普通漏斗 | C. | 烧瓶 | D. | 蒸发皿 |
分析 萃取、分液用到烧杯和分液漏斗.
解答 解:萃取、分液必须用到的仪器名称叫分液漏斗,分液时,下层液体从下口倒出,上层液体从上口倒出,
故选A.
点评 本题考查了萃取和分液实验的仪器确定,难度不大,注意分液时,下层液体从下口倒出,上层液体从上口倒出.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.某白色粉末其成分可能是碳酸钠和亚硫酸钠的一种或两种组成.请完成对该白色粉末成分的探究(可供选用的实验仪器及试剂如下).

(1)提出合理假设
假设1:该白色粉末成分为碳酸钠;
假设2:该白色粉末成分为亚硫酸钠;
假设3:该白色粉末成分为碳酸钠和亚硫酸钠的混合物.
(2)从上述仪器和试剂中选择合适的组合,一次性判断出该白色粉末的组成,其最佳连接顺序是:a-f-g-b-c-d-e(每组选用仪器和试剂限用一次).
(3)根据(2)的连接顺序进行实验,填写相应现象.

(1)提出合理假设
假设1:该白色粉末成分为碳酸钠;
假设2:该白色粉末成分为亚硫酸钠;
假设3:该白色粉末成分为碳酸钠和亚硫酸钠的混合物.
(2)从上述仪器和试剂中选择合适的组合,一次性判断出该白色粉末的组成,其最佳连接顺序是:a-f-g-b-c-d-e(每组选用仪器和试剂限用一次).
(3)根据(2)的连接顺序进行实验,填写相应现象.
| 假设方案编号 | 相应现象 |
| 假设1 | 品红试液不褪色,澄清石灰水变浑浊 |
| 假设2 | 品红试液褪色,澄清石灰水不变浑浊 |
| 假设3 | 品红试液褪色,酸性高锰酸钾溶液颜色变浅(或不褪色),澄清石灰水变浑浊 |
16.下列叙述正确的是( )
| A. | 1molH2O的质量是18g/mol | |
| B. | CH4的摩尔质量是16g | |
| C. | 3.01×1023个CO2分子的质量是22g | |
| D. | 标准状况下,1mol任何物质的体积均为22.4L |
3.下列实验操作中错误的是( )
| A. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| D. | 萃取操作时,应选择有机萃取剂 |
13.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:下列说法正确的是( )
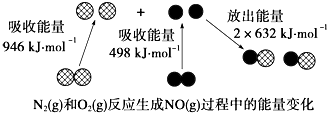

| A. | 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ | |
| B. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| C. | 通常情况下,N2(g)和O2(g)混合能直接生成NO | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
20.下列所述实验操作中,正确的是( )
| A. | 测定溶液的pH时,先将pH试纸用蒸馏水润湿,再测量 | |
| B. | 制取蒸馏水时,为防止烧瓶内产生暴沸现象,先向烧瓶中加入几片碎瓷片,再加热 | |
| C. | 分液时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 | |
| D. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
17.已知分解1molH2O2放出热量98kJ.在含有少量I-的溶液中,H2O2分解的机理为:
H2O2+I-→H2O+IO-
H2O2+IO-→H2O+O2+I-.
下列有关该反应的说法不正确的是( )
H2O2+I-→H2O+IO-
H2O2+IO-→H2O+O2+I-.
下列有关该反应的说法不正确的是( )
| A. | H2O2(l)═2H2O(g)+O2(g)△H=-196kJ•mol-1 | |
| B. | 在该反应中H2O2既做氧化剂.又做还原剂 | |
| C. | 反应速率与I-浓度有关 | |
| D. | v(H2O2)=v(H2O)=v(O2) |
18.将蓝色石蕊试纸浸入氯水中后再取出,观察到的现象是( )
| A. | 蓝色不变 | B. | 试纸呈红色 | ||
| C. | 试纸先变红,再变白 | D. | 试纸立即变白 |
 今有碱金属的两种碳酸盐和碱土金属(第二主族)的一种不溶性碳酸盐组成的混合物,取其7.560g与过量盐酸完全反应,放出CO2体积为1.344L(标况下)另取等质量的原混合物,加水搅拌,可滤出不溶性盐1.420g.
今有碱金属的两种碳酸盐和碱土金属(第二主族)的一种不溶性碳酸盐组成的混合物,取其7.560g与过量盐酸完全反应,放出CO2体积为1.344L(标况下)另取等质量的原混合物,加水搅拌,可滤出不溶性盐1.420g.