题目内容
【题目】2019年10月9日,瑞典皇家科学院宣布2019年度诺贝尔化学奖授予在锂离子电池的发展方面做出贡献的科学家。某高能![]() 电池,多应用于公共交通。电池工作时结构如图所示,电池中间是聚合物的隔膜,主要作用是在反应过程中只让
电池,多应用于公共交通。电池工作时结构如图所示,电池中间是聚合物的隔膜,主要作用是在反应过程中只让![]() 通过,电池工作时总反应可以表示为:
通过,电池工作时总反应可以表示为:![]() 。下列说法不正确( )
。下列说法不正确( )
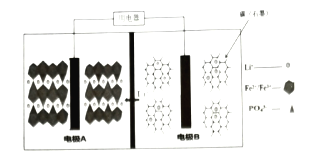
A.电池工作时,电极B为负极
B.充电时,电极A上的电势比电极B上的高
C.电池工作时,A极电极反应式:![]()
D.充电时,以铅蓄电池为电源,则电极A与![]() 电极相连
电极相连
【答案】D
【解析】
![]() →
→![]() ,该过程是化合价降低的过程,即得电子,则FePO4作氧化剂,即电极A为正极,其电极反应为:
,该过程是化合价降低的过程,即得电子,则FePO4作氧化剂,即电极A为正极,其电极反应为:![]() ;图示为电池工作的结构装置,且隔膜仅允许Li+通过,也标明了Li+的移动方向,则Li+在电极B上生成,即电极B发生
;图示为电池工作的结构装置,且隔膜仅允许Li+通过,也标明了Li+的移动方向,则Li+在电极B上生成,即电极B发生![]() →Li+的过程,该过程是失去电子的过程,则电极B作负极,其电极反应为:LixCn-xe-=xLi++Cn;据此进行作答。
→Li+的过程,该过程是失去电子的过程,则电极B作负极,其电极反应为:LixCn-xe-=xLi++Cn;据此进行作答。
A、图示为电池工作的结构装置,且隔膜仅允许Li+通过,也标明了Li+的移动方向,则Li+在电极B上生成,即电极B发生![]() →Li+的过程,该过程是失去电子的过程,则电极B作负极,A正确;
→Li+的过程,该过程是失去电子的过程,则电极B作负极,A正确;
B、充电时,电极A发生氧化反应,则电极A作阳极,即电极A与电源正极相连,则电极B与电源负极相连,电极A上的电势比电极B上的高,B正确;
C、电池工作时,A极为正极,其电极反应为:![]() ,C正确;
,C正确;
D、铅蓄电池为电源时,充电过程中,电极A与电源正极(PbO2)相连,D错误;
故选D。

【题目】工业上制取CuCl2的生产流程如下:
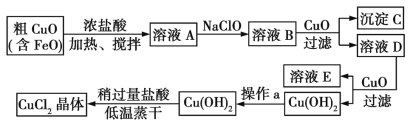
请结合下表数据,回答问题:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
溶度积(25 ℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
(1)在溶液A中加入NaClO的目的是________________________。
(2)在溶液B中加入CuO的作用是________________________________。
(3)操作a的目的是__________________________。
(4)在Cu(OH)2中加入盐酸使Cu(OH)2转化为CuCl2,采用稍过量盐酸和低温蒸干的目的是________________。