题目内容
9.对下列化学反应的热现象的说法正确的是( )| A. | 所有的放热反应不加热都能进行 | |
| B. | 任何化学反应的发生一定伴有能量变化 | |
| C. | 吸热反应和放热反应都需要加热才能发生 | |
| D. | 化学反应吸收或放出热量的多少与参加反应的物质的多少无关 |
分析 A、有些放热反应需要加热才能进行;
B、所有的反应均存在热效应;
C、反应吸放热与反应条件无关;
D、反应的热效应与物质的物质的量呈比例.
解答 解:A、有些放热反应需要加热才能进行,如煤炭的燃烧虽然是放热反应,但也需加热才能发生,故A错误;
B、所有的反应均存在热效应,不存在既不吸热也不放热的反应,故B正确;
C、反应吸放热与反应条件无关,吸热反应不一定需要加热,放热反应也不一定不需要不加热,故C错误;
D、反应的热效应与物质的物质的量呈正比,故化学反应吸收或放出热量的多少与参加反应的物质的多少有关,故D错误.
故选B.
点评 本题考查了反应吸放热的判断和与反应条件的关系,应注意的是吸热反应不一定需要加热,放热反应也不一定不需要不加热,难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
17.下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为Na>Al>O.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑨中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: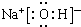 或
或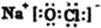 ;由②、④两种元素形成的一种气体会产生温室效应,其电子式为:
;由②、④两种元素形成的一种气体会产生温室效应,其电子式为: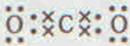 .
.
(4)有两种化合物均由①、④、⑤、⑧四种元素形成,两者之间可以相互发生化学反应,其离子反应方程式为:HSO3-+H+=H2O+SO2↑.
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
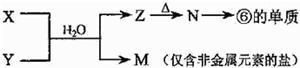
X溶液与Y溶液反应的离子方程式为Al3++3NH3+3H2O=Al(OH)3↓+3NH4+,
N→⑥的单质的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑨中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
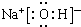 或
或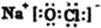 ;由②、④两种元素形成的一种气体会产生温室效应,其电子式为:
;由②、④两种元素形成的一种气体会产生温室效应,其电子式为: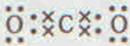 .
.(4)有两种化合物均由①、④、⑤、⑧四种元素形成,两者之间可以相互发生化学反应,其离子反应方程式为:HSO3-+H+=H2O+SO2↑.
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为Al3++3NH3+3H2O=Al(OH)3↓+3NH4+,
N→⑥的单质的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
4.某元素的一个原子形成的离子可表示为${\;}_{a}^{b}$Xn-,下列说法正确的是( )
| A. | ${\;}_{a}^{b}$Xn-含有的中子数为a+b | |
| B. | ${\;}_{a}^{b}$Xn-含有的电子数为a-n | |
| C. | X原子的质量数为a+b+n | |
| D. | 一个X原子的质量约为$\frac{b}{6.02×1{0}^{23}}$ g |
14.观察分析,符合图中变化的化学反应为( )
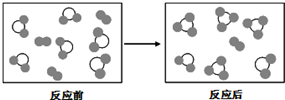

| A. | A2+3B2═2AB3 | B. | 2AB2+B2═2AB3 | C. | 2A2B+5B2=4AB3 | D. | 2AB2+B2=2AB3 |
1.下列说法不正确的是( )
| A. | △H>0、△S>0的反应在任何温度下都不能自发进行 | |
| B. | 反应NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57 kJ•mol-1之所以能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 | |
| C. | 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均不能单独作为反应自发性的判据 | |
| D. | 在其它外界条件不变的情况下,使用催化剂,可以改变化学反应进行的速率 |
18.某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.50mol•L-1NaOH溶液、0.55mol•L-1盐酸,实验尚缺少的玻璃仪器是量筒和温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否).
(3)他们记录的实验数据如下:
已知:Q=cm△t,c为4.18J•℃-1•g-1,各溶液的密度均为1g•cm-3.
①通过计算得到中和热△H=-55.2kJ/mol(保留一位小数).
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:HCl(aq)+NaOH(aq)=NaCl(aq)+2H2O(l)△H=-55.2kJ/mol.
(4)若用0.60mol•L-1NaOH溶液代替0.50mol•L-1NaOH溶液做实验,对测定结果无(填“有”或“无”,下同)影响;若用0.55mol•L-1醋酸代替0.55mol•L-1盐酸做实验,对测定结果有影响.
(5)计算结果发现本次实验测定值与正确值57.3kJ/mol有偏差,产生偏差的原因可能是②③(填序号)操作:
①量取NaOH溶液的体积时仰视读数
②用温度计测定NaOH溶液的温度后直接测定盐酸的温度
③分多次把NaOH溶液倒入装盐酸的小烧杯中.
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.50mol•L-1NaOH溶液、0.55mol•L-1盐酸,实验尚缺少的玻璃仪器是量筒和温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否).
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50 mL 0.50 mol•L-1 NaOH溶液 | 50 mL 0.55 mol•L-1 HCl溶液 | 20℃ | 23.2℃ | |
| ② | 50 mL 0.50 mol•L-1 NaOH溶液 | 50 mL 0.55 mol•L-1 HCl溶液 | 20℃ | 23.4℃ | |
①通过计算得到中和热△H=-55.2kJ/mol(保留一位小数).
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:HCl(aq)+NaOH(aq)=NaCl(aq)+2H2O(l)△H=-55.2kJ/mol.
(4)若用0.60mol•L-1NaOH溶液代替0.50mol•L-1NaOH溶液做实验,对测定结果无(填“有”或“无”,下同)影响;若用0.55mol•L-1醋酸代替0.55mol•L-1盐酸做实验,对测定结果有影响.
(5)计算结果发现本次实验测定值与正确值57.3kJ/mol有偏差,产生偏差的原因可能是②③(填序号)操作:
①量取NaOH溶液的体积时仰视读数
②用温度计测定NaOH溶液的温度后直接测定盐酸的温度
③分多次把NaOH溶液倒入装盐酸的小烧杯中.
19.某温度下,0.02mol•L-1NaHSO3溶液的pH=3.下列说法正确的是( )
| A. | 加水稀释10倍后,溶液的pH=4 | |
| B. | c(SO32-)+c(OH-)=c(H2SO3)+c(HSO3-) | |
| C. | 2c(SO32-)+c(HSO3-)+c(H2SO3)=0.02mol•L-1 | |
| D. | $\frac{c({H}^{+})•c(S{{O}_{3}}^{2-})}{c(HS{{O}_{3}}^{-})}$约为5×10-5 mol•L-1 |

 ③
③ 、
、 .
. .
. .
.