题目内容
11.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的质量增加了8.1g,则此反应的反应速率v(X)可表示为( )| A. | v(NH3)=0.010 mol/( L•s) | B. | v(O2)=0.001 mol/( L•s) | ||
| C. | v(NO)=0.001 mol/( L•s) | D. | v(H2O)=0.045 mol/( L•s) |
分析 根据n=$\frac{m}{M}$、v=$\frac{△n}{\frac{V}{△t}}$计算v(H2O),在利用速率之比等于化学计量数之比计算其它物质表示的速率,据此判断.
解答 解:半分钟后,水蒸气的质量增加了8.1g,水蒸气的物质的量增加了n=$\frac{m}{M}$=$\frac{8.1g}{18g/mol}$=0.45mol,则v(H2O)=$\frac{△n}{\frac{V}{△t}}$=$\frac{0.45mol}{\frac{10L}{30s}}$=0.0015mol/(L•s),
A.速率之比等于化学计量数之比,故v(NH3)=$\frac{2}{3}$v(H2O)=$\frac{2}{3}$×0.0015mol/(L•s)=0.001mol/(L•s),故A错误;
B.速率之比等于化学计量数之比,故v(O2)=$\frac{5}{6}$v(H2O)=$\frac{5}{6}$×0.0015mol/(L•s)=0.00125mol/(L•s),故B错误;
C.速率之比等于化学计量数之比,故v(NO)=$\frac{2}{3}$v(H2O)=$\frac{2}{3}$×0.0015mol/(L•s)=0.001mol/(L•s),故C正确;
D.半分钟后,水蒸气的物质的量增加了0.45mol,则v(H2O)=$\frac{0.45mol}{\frac{10L}{30s}}$=0.0015mol/(L•s),故D错误;
故选C.
点评 本题考查化学反应速率的有关计算,比较基础,难度不大,化学反应速率常用计算方法有定义法与化学计量数法,注意根据情况选择合适的计算方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列说法中正确的是( )
| A. | 已知BF3键角为120°,则SnBr2键角小于120° | |
| B. | SO2是直线型分子 | |
| C. | PCl5是三角锥形分子 | |
| D. | 四氨合铜离子中铜离子的配位数为2 |
2.一定量的铝与过量的稀盐酸反应时,为了加快反应速率,但又不影响生成的氢气总量,可以采取的措施是( )
| A. | 升高温度 | B. | 加入适量的水 | ||
| C. | 加入少量CuSO4溶液 | D. | 加入浓度较大的盐酸 |
19.图所示装置中,已知电子由b极沿导线流向锌.下列判断正确的是( )
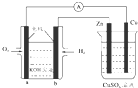

| A. | 该装置中Zn极为阳极 | |
| B. | 一段时间后铜片上质量增加 | |
| C. | a极反应的电极反应式为:O2+4e-+2H2O═4OH- | |
| D. | 当铜极的质量变化为32g时,b极上消耗的O2的体积为11.2 L |
6.在2L密闭容器中,发生3A+B=2C (均为气体)的反应,若最初加入A和B都是4mol,A的平均反应速率是0.12mol/(L.s),则10s后容器中的B的物质的量是( )
| A. | 1.6mol | B. | 3.2mol | C. | 3.6mol | D. | 2.8mol |
16.通过下列方法测定1.80g金属Sn样品的纯度.
①将样品溶于盐酸:Sn+2HCl═SnCl2+H2↑;
②加过量FeCl3溶液:SnCl2+2FeCl3═SnCl4+2FeCl2;
③再用酸性KMnO4反应生成的Fe2+,用去0.1000mol/L的KMnO4溶液60.00mL,反应的离子方程式为:MnO4-+
5Fe2++8H+═Mn2++5Fe3++4H2O.
计算金属Sn样品的纯度为( )
①将样品溶于盐酸:Sn+2HCl═SnCl2+H2↑;
②加过量FeCl3溶液:SnCl2+2FeCl3═SnCl4+2FeCl2;
③再用酸性KMnO4反应生成的Fe2+,用去0.1000mol/L的KMnO4溶液60.00mL,反应的离子方程式为:MnO4-+
5Fe2++8H+═Mn2++5Fe3++4H2O.
计算金属Sn样品的纯度为( )
| A. | 99.2% | B. | 49.6% | C. | 96.2% | D. | 46.6% |
20.互为同分异构体的一组是( )
| A. | ${\;}_1^1$H与${\;}_1^2$H | B. | O2与O3 | C. | 乙醇与二甲醚 | D. | 甲烷与丁烷 |
14.下列物质中,不属于酸性氧化物的是( )
| A. | NO2 | B. | SiO2 | C. | Mn2O7 | D. | SO2 |
 某化学兴趣小组用如图所示装置进行电化学原理的实验探究,试回答下列问题:
某化学兴趣小组用如图所示装置进行电化学原理的实验探究,试回答下列问题: