题目内容
1.在一个小烧杯里,加入约20g已研磨成粉末的氢氧化钡晶体[Ba(OH)2•8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10g NH4Cl晶体,并立即用玻璃棒迅速搅拌,如图所示.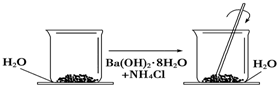
试回答下列问题:
(1)实验中要立即用玻璃棒迅速搅拌的原因是使反应物充分混合,迅速发生反应,使体系的温度降低.
(2)如果实验中没有看到“结冰”现象,可能的原因是①反应物未进行快速搅拌;②玻璃片上滴加的水太多;③氢氧化钡晶体已部分失水;④环境温度太高;⑤试剂用量太少;⑥氢氧化钡晶体未研成粉末(其他答案合理均正确)(答出3个或3个以上原因).
(3)如果没有看到“结冰”现象,为说明该反应吸热,我们还可以采取的方式是①用皮肤感受,感觉很凉;②用温度计来检验,发现温度降低(答出两种方案).
(4)实验中即使不“结冰”,提起烧杯的时候,发现烧杯与玻璃片也“黏在一起了”,原因是水排开了烧杯底部与玻璃片之间的空气,在大气压的作用下,烧杯与玻璃片黏在一起了
(5)试用简单的方法说明烧杯与玻璃片之间是因为“结冰”而黏在一起的:将烧杯和玻璃片提起,从侧面轻推玻璃片,看能否从侧面相对滑动,若不能,则是由于“结冰”而黏在一起的.
分析 (1)玻璃棒的搅拌作用是使混合物混合均,让化学反应快速发生;
(2)根据反应是否充分进行分析;
(3)通过玻璃片上结冰现象、烧杯和底部的玻璃片粘在一起、用手触摸烧杯外壁有冰凉的感觉、用温度计测混合物的温度看是否降温等方法可以确定反应是吸热的;
(4)根据水排开了烧杯底部与玻璃片之间的空气,在外压的作用下,烧杯与玻璃片也“黏在一起了”;
(5)结冰后玻璃片与烧杯会固定在一起,如果没有结冰,从侧面轻推玻璃片,玻璃片能发生相对滑动,据此进行解答.
解答 解:(1)氢氧化钡晶体[Ba(OH)2•8H2O]和氯化铵晶体之间的反应是固体之间的反应,搅拌可使混合物充分接触并发生反应,使体系的温度降低;
故答案为:使反应物充分混合,迅速发生反应,使体系的温度降低;
(2)①反应物未进行快速搅拌;②玻璃片上滴加的水太多;③氢氧化钡晶体已部分失水;④环境温度太高;⑤试剂用量太少;⑥氢氧化钡晶体未研成粉末,可能看不到“结冰”现象,
故答案为:①反应物未进行快速搅拌;②玻璃片上滴加的水太多;③氢氧化钡晶体已部分失水;④环境温度太高;⑤试剂用量太少;⑥氢氧化钡晶体未研成粉末(其他答案合理均正确);
(3)氢氧化钡晶体和氯化铵的反应是吸热反应,可以根据用手触摸烧杯外壁看是否变凉、用温度计测混合物的温度看是否降温、玻璃片上结冰现象、烧杯和底部的玻璃片粘在一起等现象来证明;
故答案为:①用皮肤感受,感觉很凉;②用温度计来检验,发现温度降低;
(4)水排开了烧杯底部与玻璃片之间的空气,外压大于内压,烧杯与玻璃片黏在一起了;
故答案为:水排开了烧杯底部与玻璃片之间的空气,在大气压的作用下,烧杯与玻璃片黏在一起了;
(5)由于水排开了烧杯底部和玻璃片之间的空气,在大气压作用下烧杯也可能与玻璃片粘在一起,可将烧杯和玻璃片提起,从侧面轻推玻璃片,通过玻璃片能否发生滑动来判断,
故答案为:将烧杯和玻璃片提起,从侧面轻推玻璃片,看能否从侧面相对滑动,若不能,则是由于“结冰”而黏在一起的.
点评 本题考查了化学反应中的能量变化以及吸热反应,以Ba(OH)2•8H2O与NH4Cl固体的反应为背景考查了分析问题、解决问题的能力和实验设计能力,反应放出或吸收的热量可以通过触觉感知,也可以通过温度计测量,题目难度不大.

| A. | XY3 | B. | X2Y3 | C. | X3Y | D. | XY |
| A. | 4L 0.5mol•L-1NaCl溶液 | B. | 2L 0.3mol•L-1的Na2SO4溶液 | ||
| C. | 0.8L 0.4mol•L-1NaOH溶液 | D. | 1L 0.25mol•L-1的Na3PO4溶液 |
| A. | 氢氧化铁胶体和氯化铁溶液的本质区别为是否具有丁达尔效应 | |
| B. | 氯化铁溶液呈电中性,氢氧化铁胶体带有电荷 | |
| C. | 纳米材料的微粒一般从几纳米到几十纳米,因此纳米材料是胶体 | |
| D. | 氯化铁溶液能使血液凝聚沉降 |
| A. | 常温常压下,11.2LCO2所含的原子数为1.5NA | |
| B. | 常温常压下,48gO2与O3混合物含有的氧原子数为3NA | |
| C. | 标准状况下,22.4LCCl4中所含分子数为NA | |
| D. | 标准状况下,18g水所含原子数为NA |
| A. | 蒸馏法 | B. | 电渗析法 | C. | 热蒸发法 | D. | 离子交换法 |
 某学生在实验室分别取50mL0.50mol/L盐酸和50mL0.55mol/LNaOH溶液用如图所示装置进行测定中和热的实验,并将实验数据记录如下:
某学生在实验室分别取50mL0.50mol/L盐酸和50mL0.55mol/LNaOH溶液用如图所示装置进行测定中和热的实验,并将实验数据记录如下:| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol.
(2)经数据处理,t2-t1=3.4℃.则该实验测得的中和热△H=-56.8kJ/mol.
(3)假定该学生的操作完全同上,实验中改用100mL 0.50mol/L盐酸跟100mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量不相等(填“相等”或“不相等”),所求中和热相等(填“相等”或“不相等”).