题目内容
20.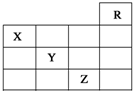 如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )
如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )①X的气态氢化物与Y最高价氧化物对应的水化物的溶液能发生反应生成盐
②同浓度的Y、Z的气态氢化物的水溶液的酸性Y<Z
③Z的单质常温下是深红棕色液体,具有氧化性
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素.
| A. | 只有③ | B. | 只有①④ | C. | 只有①②③④ | D. | ①②③④⑤ |
分析 由元素周期表的一部分及元素的位置可知,则R为He、X为氮元素、Y为硫元素、Z为Br元素,
①X的气态氢化物与Y最高价氧化物对应的水化物分别为氨气、硫酸;
②Y、Z的气态氢化物分别为H2S、HBr;
③溴常温下为液体,可与铁粉反应生成溴化铁;
④Br的原子序数比S大19;
⑤Br位于第四周期.
解答 解:由元素周期表的一部分及元素的位置可知,则R为He、X为氮元素、Y为硫元素、Z为Br元素,
①X的气态氢化物与Y最高价氧化物对应的水化物反应可以生成硫酸铵,为铵盐,故正确;
②Y、Z的气态氢化物分别为H2S、HBr,水溶液中HBr完全电离,而H2S不能,则同浓度的Y、Z的气态氢化物的水溶液的酸性Y<Z,故正确;
③溴常温下为液体,可与铁粉反应生成溴化铁,可知Br得到电子具有氧化性,故正确;
④Br的原子序数比氯原子的原子序数大18,氯原子序数比硫原子大1,故Br元素序数比S的原子序数大19,故正确;
⑤Br处于第四周期,所在的周期中含有18种元素,周期表中第六周期有32种元素,故错误;
故选C.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、元素化合物性质为解答的关键,侧重分析与应用能力的考查,注意周期表的结构,题目难度不大.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
10. 在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示.下列说法不正确的是( )
在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示.下列说法不正确的是( )
 在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示.下列说法不正确的是( )
在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示.下列说法不正确的是( )| A. | 该反应的化学方程式为5A+4B?4C | |
| B. | 2min时,该反应达到平衡,此时A、B、C的浓度比为5:4:4 | |
| C. | 用B的浓度变化表示2min内的速率为2mol/(L•min) | |
| D. | 2min前,正反应速率逐渐减小,逆反应速率逐渐增大 |
11.以下叙述错误的是( )
| A. | 氢气与氯气反应后,体系的能量降低 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | 若生成物的总能量高于反应物的总能量,则反应过程吸收能量 | |
| D. | 化学反应的实质是旧化学键的断裂和新化学键的形成 |
8. 在2L的恒容密闭容器中,发生反应:A(g)+B(g)?2C(g)+D(s)△H=-a kJ•mol-1,实验内容和结果分别如表和如图所示.下列说法正确的是( )
在2L的恒容密闭容器中,发生反应:A(g)+B(g)?2C(g)+D(s)△H=-a kJ•mol-1,实验内容和结果分别如表和如图所示.下列说法正确的是( )
 在2L的恒容密闭容器中,发生反应:A(g)+B(g)?2C(g)+D(s)△H=-a kJ•mol-1,实验内容和结果分别如表和如图所示.下列说法正确的是( )
在2L的恒容密闭容器中,发生反应:A(g)+B(g)?2C(g)+D(s)△H=-a kJ•mol-1,实验内容和结果分别如表和如图所示.下列说法正确的是( )| 实验 序号 | 温度 | 起始物质的量 | 热量 变化 | |
| A | B | |||
| Ⅰ | 600℃ | 1 mol | 3 mol | 96 kJ |
| Ⅱ | 800℃ | 0.5 mol | 1.5mol | -- |
| A. | 实验Ⅰ中,10 min内平均速率v(B)=0.06 mol•L-1•min-1 | |
| B. | 600℃时,上述方程式中a=160 | |
| C. | 600℃时,该反应的平衡常数是0.45 | |
| D. | 向实验Ⅱ的平衡体系中再充入0.5 mol A和1.5 mol B,A的转化率不变 |
15.根据原子结构的相关知识可知,不同种元素的本质区别是( )
| A. | 质子数不同 | B. | 中子数不同 | C. | 电子数不同 | D. | 质量数不同 |
12.下列各组离子在一定条件下能够大量共存的是( )
| A. | 无色溶液:Cu2+、K+、MnO4-、SO42- | |
| B. | 能溶解Al2O3的溶液:Na+、Ca2+、HCO3-、NO3- | |
| C. | 常温下c(OH-)=1×10-13mol•L-1的溶液:NH4+、Al3+、SO42-、Cl- | |
| D. | 含1.2 mol•L-1 NO3-的溶液:H+、Fe2+、Mg2+、Br- |
9.为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:

部分含钒物质在水中的溶解性如下:
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$5Al2O3+6V.
(2)图中所示滤液中含钒的主要成分为VOSO4(写化学式).
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式NH4++VO3-=NH4VO3↓;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度.根据如图判断最佳控制氯化铵系数和温度为4、80℃.

(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,完成反应的离子方程式为2VO2++H2C2O4+2H+=2VO2++2CO2↑+2H2O;
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2++V2++2H+$?_{充电}^{放电}$VO2++H2O+V3+,电池充电时阳极的电极反应式为VO2++H2O-e-=VO2++2H+.

部分含钒物质在水中的溶解性如下:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
(1)工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$5Al2O3+6V.
(2)图中所示滤液中含钒的主要成分为VOSO4(写化学式).
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式NH4++VO3-=NH4VO3↓;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度.根据如图判断最佳控制氯化铵系数和温度为4、80℃.

(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,完成反应的离子方程式为2VO2++H2C2O4+2H+=2VO2++2CO2↑+2H2O;
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2++V2++2H+$?_{充电}^{放电}$VO2++H2O+V3+,电池充电时阳极的电极反应式为VO2++H2O-e-=VO2++2H+.
10.下列物质属于人工合成聚合物的是( )
| A. | 蛋白质 | B. | 蚕丝 | C. | 棉花 | D. | 聚氯乙烯 |