题目内容
15.根据原子结构的相关知识可知,不同种元素的本质区别是( )| A. | 质子数不同 | B. | 中子数不同 | C. | 电子数不同 | D. | 质量数不同 |
分析 根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,进行解答.
解答 解:根据元素的概念,元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的微粒是质子数即元素的最本质区别是质子数不同.
故选A.
点评 本题主要考查元素概念的理解与掌握,并应用于解题,属于基础知识,题目难度不大.

练习册系列答案
相关题目
5.下列试剂中,能鉴别乙醇、乙酸和葡萄糖三种溶液的是( )
| A. | 水 | B. | 新制氢氧化铜浊液 | ||
| C. | 碳酸钠溶液 | D. | 紫色石蕊试液 |
6.有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为( )
| A. | A>B>C>D | B. | B>D>C>A | C. | C>A>B>D | D. | A>C>D>B |
3.下列叙述正确的是( )
| A. | 铅蓄电池放电过程中,正极质量增加,负极质量减小 | |
| B. | 将0.1 mol•L-1的NH3•H2O溶液加水稀释,$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$比值减小 | |
| C. | NaHCO3溶于水,溶液中存在电离平衡 | |
| D. | CaCO3(s)═CaO(s)+CO2(g),△H>0,该反应在任意温度下都能自发进行 |
20.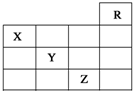 如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )
如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )
①X的气态氢化物与Y最高价氧化物对应的水化物的溶液能发生反应生成盐
②同浓度的Y、Z的气态氢化物的水溶液的酸性Y<Z
③Z的单质常温下是深红棕色液体,具有氧化性
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素.
 如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )
如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )①X的气态氢化物与Y最高价氧化物对应的水化物的溶液能发生反应生成盐
②同浓度的Y、Z的气态氢化物的水溶液的酸性Y<Z
③Z的单质常温下是深红棕色液体,具有氧化性
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素.
| A. | 只有③ | B. | 只有①④ | C. | 只有①②③④ | D. | ①②③④⑤ |
5.下列化学反应中,属于氧化还原反应的是( )
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | NH3+HCl=NH4Cl | ||
| C. | 2Fe(OH)3$\frac{\underline{\;加热\;}}{\;}$Fe2O3+3H2O | D. | NaOH+HNO3=NaNO3+H2O |
 某学生实验小组,用稀硫酸和稀氢氧化钠溶液在如图所示的装置中,进行中和反应反应热的测定.请回答下列问题:
某学生实验小组,用稀硫酸和稀氢氧化钠溶液在如图所示的装置中,进行中和反应反应热的测定.请回答下列问题: