题目内容
5.日本福岛第一核电站泄漏出微量的钚(Pu),下列关${\;}_{94}^{239}$Pu叙述正确的是( )| A. | 质子数是94 | B. | 原子序数是239 | C. | 质量数是94 | D. | 中子数是239 |
分析 根据原子符号中,左下脚的数字为质子数,左上角的数字为质量数,中子数=质量数-质子数,质子数=原子序数=核电荷数=核外电子数.
解答 解:A.${\;}_{94}^{239}$Pu的质子数为94,故A正确;
B.${\;}_{94}^{239}$Pu的质子数为94,所以原子序数为94,故B错误;
C.${\;}_{94}^{239}$Pu的质量数是239,故C错误;
D.${\;}_{94}^{239}$Pu的质子数为94,质量数是239,中子数=239-94=145,故D错误;
故选A.
点评 本题主要考查了原子符号的含义,中子数=质量数-质子数以及质子数=原子序数=核电荷数=核外电子数,难度不大.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
13.将纯锌片和纯铜片按如图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
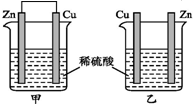

| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 两烧杯中溶液的酸性均减弱 | D. | 产生气泡的速率甲比乙慢 |
20. 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.下如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.下如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.下如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.下如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A. | 该物质与SN2互为同素异形体 | |
| B. | 该物质的分子中既有极性键又有非极性键 | |
| C. | 该物质可能是离子化合物 | |
| D. | 该物质的一个分中含有9个N-S键 |
10.用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A. | 常温常压下,22.4 LCO2含有的原子数为3NA | |
| B. | 0.1 mol Na2O2固体含有的阴、阳离子总数是0.3NA | |
| C. | 1.8gNH4+含有的质子数为NA | |
| D. | 标准状况下,2.24 L NO与1.12 L O2混合,所得气体中分子数为0.15NA |
17.几种短周期元素的原子半径及主要化合价如表:
下列说法正确的是( )
| 元素代号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
| A. | X的最高价氧化物的水化物碱性比Y的弱 | |
| B. | Y既可以和酸反应又可以和碱反应,且化合价变化相同 | |
| C. | 常温下,Z单质可以与L的氢化物溶液反应置换出L单质 | |
| D. | X、M分别与Q形成的化合物中所含化学键类型相同 |
15.下列离子组一定能大量共存的是( )
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 由水电离出c(H+)=10-3 mol•L-1的溶液中:Na+、AlO2-、NO3-、HCO3- | |
| C. | 无色溶液中可能大量存在Al3+、NH4+、Cl-、S2- | |
| D. | pH=12的溶液:K+、Na+、CH3COO-、Br- |
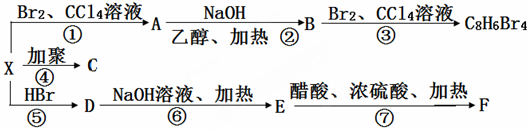
 用化学用语回答下面的问题
用化学用语回答下面的问题
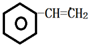 ,C的结构简式:
,C的结构简式: .
.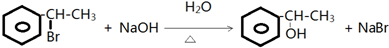 .
.