题目内容
17.已知2SO2+O2?2SO3是一个正反应放热的可逆反应.如果反应在密闭容器中进行,则下列有关途述正确的是( )| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 升高温度可加快逆反应速率但不能改变正反应速率 | |
| C. | 一定条件下,SO2可100%转化为SO3 | |
| D. | 任何条件下,反应达到平衡,SO2的浓度一定等于SO3的浓度 |
分析 A.催化剂能增大反应速率,缩短反应到达平衡的时间;
B.升高温度,能增大正逆反应速率;
C.可逆反应中反应物不能完全转化为生成物;
D.反应达到平衡状态时,二氧化硫和三氧化硫浓度不一定相等.
解答 解:A.催化剂能增大反应速率,缩短反应到达平衡的时间,所以能提高生产效率,故A正确;
B.升高温度,增大活化分子百分数,所以能增大正逆反应速率,故B错误;
C.可逆反应中存在反应限度,所以反应物不能完全转化为生成物,故C错误;
D.反应达到平衡状态时,二氧化硫和三氧化硫浓度不一定相等,与反应物初始浓度及转化率有关,故D错误;
故选A.
点评 本题考查可逆反应、化学反应速率影响因素等知识点,明确外界条件对反应速率影响原理是解本题关键,易错选项是A,注意催化剂只能改变反应速率不影响平衡移动,为易错点.

练习册系列答案
相关题目
17.松节油结构如图所示,在浓硫酸、加热条件下发生消去反应,最多可以生成几种有机产物( )
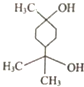

| A. | 4种 | B. | 5种 | C. | 8种 | D. | 9种 |
8.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下22.4L氯气通入足量水中反应,转移的电子数为NA | |
| B. | 乙烯和氮气组成的28g混合气体中含有NA个分子 | |
| C. | 1molNa2O2中阳离子和阴离子数均为2NA | |
| D. | 1molFeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
12.下列说法中正确的是( )
| A. | 近期媒体报道的某白酒中添加的塑化剂是对人体健康无害的物质 | |
| B. | 尽量使用含12C的产品,减少使用含13C或14C的产品符合“低碳经济”宗旨 | |
| C. | 大量二氧化碳气体的排放是形成酸雨的主要原因 | |
| D. | 使用太阳能、风能、潮汐能等能源能减少PM2.5的污染 |
6.常温下,下列有关叙述正确的是( )
| A. | 水的离子积KW只与温度有关,但水的电离程度一定会受外加酸、碱、盐的影响 | |
| B. | 若HA的Ka=1.7×10-5,BOH的Kb=1.7×10-5,则HA溶液中的c(H+)与BOH中的c(OH-)相等 | |
| C. | 将0.2mol/L HA溶液和0.1mol/L NaOH溶液等体积混合,则反应后的混合液中:c(OH-)+c(A-)=c(H+)+c(HA) | |
| D. | Mg(OH)2能溶于NH4Cl浓溶液的主要原因是NH4+结合OH-使沉淀溶解平衡发生正向移动 |
7.下列实验操作中正确的是( )
| A. | 用湿润的pH试纸测定某稀醋酸溶液的pH | |
| B. | 做完银镜反应的试管可以用氨水来洗涤 | |
| C. | 如果苯酚浓溶液沾到皮肤上,应立即用酒精擦洗 | |
| D. | 为了除去苯中混有的少量苯酚,加入足量浓溴水,充分搅拌后过滤分离 |

 .
.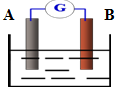 如图为某原电池装置:
如图为某原电池装置: .
. CH3COOC2H5+H2O,该反应类型是酯化(取代)反应.
CH3COOC2H5+H2O,该反应类型是酯化(取代)反应. 2CH3CHO+2H2O.
2CH3CHO+2H2O.