题目内容
13.已知化合物NH5的结构和NH4Cl相似,下列关于NH5的下列说法中正确的是( )| A. | NH5是共价化合物 | |
| B. | NH5的电子式为NH4+[:H]- | |
| C. | NH5中氢元素呈价+1和-1价 | |
| D. | NH5与水发生氧化还原反应,置换出氢气 |
分析 根据其电子式为 ,通过其电子式判断化合物的类型及化学键类型,阴阳离子间存在离子键,非金属原子间存在共价键,据此分析解答.
,通过其电子式判断化合物的类型及化学键类型,阴阳离子间存在离子键,非金属原子间存在共价键,据此分析解答.
解答 解:A、根据电子式知,该物质中含有阴阳离子,所以是离子化合物,故A错误;
B、其电子式为 ,故B错误;
,故B错误;
C、氢离子和铵根离子间存在离子键,铵根离子中氢是+1价和阴离子中的氢是-1,故C正确;
D、NH5与水发生氧化还原反应,不是置换反应,故D错误.
故选C.
点评 本题考查了离子键、共价键、离子化合物、共价化合物的判断和反应基本类型的确定,难度不大,注意离子化合物中可能含有共价键,但共价化合物中一定不含离子键.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
3.下表是元素周期表的一部分,表中的每个字母代表一种短周期元素.
(1)a元素和c元素可以形成的气体,其化学式为NH3;
(2)e的元素符号是Na;
(3)b元素原子的最外层电子数为4;
(4)b、c、d三种元素的非金属性逐渐增强(填“减弱”或“增强”);
(5)d元素和f元素均可形成气态氢化物,其稳定性为H2d大于H2f (填“大于”或“小于”).
(6)上述七种元素的最高价氧化物的水合物中,碱性最强的是NaOH,酸性最强的是HClO4,既有酸性又有碱性的是Al(OH)3(写化学式)
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | d | |||||
| 3 | e | g | f | |||||
(2)e的元素符号是Na;
(3)b元素原子的最外层电子数为4;
(4)b、c、d三种元素的非金属性逐渐增强(填“减弱”或“增强”);
(5)d元素和f元素均可形成气态氢化物,其稳定性为H2d大于H2f (填“大于”或“小于”).
(6)上述七种元素的最高价氧化物的水合物中,碱性最强的是NaOH,酸性最强的是HClO4,既有酸性又有碱性的是Al(OH)3(写化学式)
1.有两种气态烃的混合物1L,完全燃烧可得同温同压下的3.8L二氧化碳和3.6L水蒸气,这两种烃可能是( )
| A. | C2H4、C4H6 | B. | C2H2、C4H6 | C. | C3H4、C4H8 | D. | C3H4、C3H6 |
8.有A、B、C、D四种金属.将A与B用导线连接起来浸入稀硫酸中,B上有气泡产生;将A、D分别投入到等浓度的稀盐酸中,D比A反应剧烈;将Cu浸入B的盐溶液中,无明显变化;如果把Cu浸入C的盐溶液中,有金属C析出.据此判断它们的活动性由强到弱顺序是( )
| A. | C>B>A>D | B. | D>A>B>C | C. | D>B>A>C | D. | B>A>D>C |
5.如图,下列装置能产生有效电流的是( )
| A. | 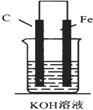 | B. | 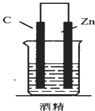 | C. | 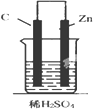 | D. |  |
 小明同学为了制得纯净而干燥的氯气,对课本上的实验方案进行了改进.在发生装置和收集装置之间添加了盛有饱和食盐水和浓硫酸的洗气瓶(如图).请回答:
小明同学为了制得纯净而干燥的氯气,对课本上的实验方案进行了改进.在发生装置和收集装置之间添加了盛有饱和食盐水和浓硫酸的洗气瓶(如图).请回答: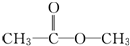
 或
或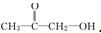 (写出结构简式).
(写出结构简式).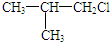 化合物有三个峰,而化合物CH3CH=CHCl却得到氢原子给出的6个信号峰.根据原子在空间的排列方式的不同,写出CH3CH=CHCl 分子的空间异构体:
化合物有三个峰,而化合物CH3CH=CHCl却得到氢原子给出的6个信号峰.根据原子在空间的排列方式的不同,写出CH3CH=CHCl 分子的空间异构体: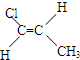
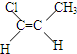 .
.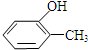 ,
, ,
,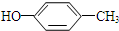 ,对应在PMR谱上观察到氢原子所给出的峰的情况及比例:1:1:1:1:1:3;1:1:1:1:1:3;1:2:2:3.
,对应在PMR谱上观察到氢原子所给出的峰的情况及比例:1:1:1:1:1:3;1:1:1:1:1:3;1:2:2:3.