题目内容
(9分)(1)常温下,有0.1mol/L的氨水和0.1mol/L的氢氧化钠溶液,回答下列问题:
①pH 值:氨水 氢氧化钠(填“<” 、“="”" 或 “>”)
②两种碱溶液均能与盐酸反应生成盐,等体积的上述两溶液与等浓度的盐酸溶液恰好反应呈中性, 消耗的盐酸多。反应生成的氯化铵溶液呈 (填“酸性” 、“中性” 或 “碱性”),其原因是(用离子方程式表示)
③向氨水溶液中加入一定量的盐酸溶液,当测得溶液的pH=7时,溶液中离子的浓度大小为
(选填字母,下同),当测得溶液的pH>7时,溶液中离子的浓度大小为 。
a.c(NH4+)>c(Cl—)>c(OH—)>c(H+) b.c(NH4+) = c(Cl—)>c(OH—) =c(H+)
c.c(Cl—)>c(NH4+)>c(H+)>c(OH—) d.c(NH4+)>c(Cl—)>c(H+)>c(OH—)
(2)向盛有1mL0.1mol/LMgCl2溶液的试管中滴加2滴2mol/L KOH溶液,有白色沉淀生成,再滴加2滴0.1mol/L FeCl3溶液,静置。可以观察到的现象是 ,产生该现象的原因是(用离子方程式和简要文字表达)
①pH 值:氨水 氢氧化钠(填“<” 、“="”" 或 “>”)
②两种碱溶液均能与盐酸反应生成盐,等体积的上述两溶液与等浓度的盐酸溶液恰好反应呈中性, 消耗的盐酸多。反应生成的氯化铵溶液呈 (填“酸性” 、“中性” 或 “碱性”),其原因是(用离子方程式表示)
③向氨水溶液中加入一定量的盐酸溶液,当测得溶液的pH=7时,溶液中离子的浓度大小为
(选填字母,下同),当测得溶液的pH>7时,溶液中离子的浓度大小为 。
a.c(NH4+)>c(Cl—)>c(OH—)>c(H+) b.c(NH4+) = c(Cl—)>c(OH—) =c(H+)
c.c(Cl—)>c(NH4+)>c(H+)>c(OH—) d.c(NH4+)>c(Cl—)>c(H+)>c(OH—)
(2)向盛有1mL0.1mol/LMgCl2溶液的试管中滴加2滴2mol/L KOH溶液,有白色沉淀生成,再滴加2滴0.1mol/L FeCl3溶液,静置。可以观察到的现象是 ,产生该现象的原因是(用离子方程式和简要文字表达)
(1)①< ② NaOH 酸性 NH4++H2O NH3.H2O+H+ ③ b a
NH3.H2O+H+ ③ b a
(2)白色沉淀转变为红褐色 3Mg(OH)2 + 2Fe3+ = 2Fe(OH)3 + 3Mg2+ ,相同条件下Fe(OH)3 溶解度小于 Mg(OH)2溶解度 ,使 Mg(OH)2溶解平衡移动,生成更难溶Fe(OH)3。
 NH3.H2O+H+ ③ b a
NH3.H2O+H+ ③ b a(2)白色沉淀转变为红褐色 3Mg(OH)2 + 2Fe3+ = 2Fe(OH)3 + 3Mg2+ ,相同条件下Fe(OH)3 溶解度小于 Mg(OH)2溶解度 ,使 Mg(OH)2溶解平衡移动,生成更难溶Fe(OH)3。
(1)氨水是弱碱,氢氧化钠是强碱,在浓度相等的条件下,氨水的碱性弱于氢氧化钠的。和盐酸恰好反应后生成的氯化铵水解显酸性,而氯化钠不水解,显中性。溶液的pH=7,则c(OH—) =c(H+),根据电荷守恒c(NH4+)+ c(H+)= c(Cl—)+c(OH—)可知c(NH4+) = c(Cl—),即选项b正确。若溶液的pH>7,则c(OH—) >c(H+),选项a正确。
(2)因为氢氧化镁的溶解度大于氢氧化铁的,根据沉淀转化的原理可知,氢氧化镁将转化为更难溶的氢氧化铁。
(2)因为氢氧化镁的溶解度大于氢氧化铁的,根据沉淀转化的原理可知,氢氧化镁将转化为更难溶的氢氧化铁。

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
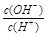 =1×10-6,下列叙述正确的是
=1×10-6,下列叙述正确的是