题目内容
【题目】兴趣小组探究锌片与盐酸、醋酸反应时,浓度或温度对反应速率的影响,他们准备了以下化学用品:0.20mol/L与0.40mol/L的HCl溶液、0.2mol/L与0.40mol/L的CH3COOH溶液、0.10mol/LCuCl2、锌片(形状、大小、质量相同)、秒表、碳棒、导线、烧杯、几支试管和胶头滴管,酸液温度控制为298K和308K。
酸液都取足量、相同体积,请你帮助完成下面实验设计表(表中不留空格):
实验编号 | 温度(K) | 盐酸浓度 | 醋酸浓度 | 实验目的 |
① | 298 | 0.20mol/L |
| a.实验①和②是探究_____对锌与盐酸反应速率的影响; b.实验①和③是探究_____对锌与盐酸反应速率的影响; c.实验①和④是探究相同温度下,相同 浓度的盐酸、醋酸与锌反应速率的区别 |
② | 308 | 0.20mol/L |
| |
③ | 298 | 0.40mol/L |
| |
④ | ______ |
| 0.20mol/L |
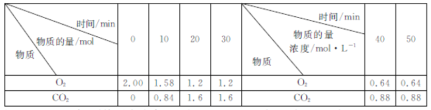
(2)若(1)中实验①锌片消失的时间是20s,则锌片剩余质量与时间关系图如下图:
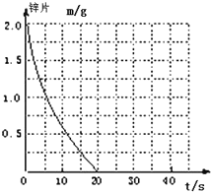
假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同、浓度相同时,醋酸的平均反应速度是盐酸的1/2.请你在此图中大致画出“实验②”(用实线)、“实验④中醋酸实验”(用虚线)的锌片质量与时间关系曲线.____________________________
(3)某实验小组在做(1)中实验④时误加少量0.10mol/LCuCl2溶液,发现反应速率与(1)中实验①接近,加少量0.10mol/LCuCl2溶液后速率变快的原因是_________________。
【答案】不同温度 不同浓度 298 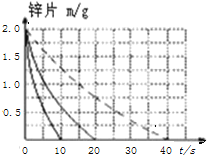 Zn和被Zn置换出的Cu、电解质溶液构成Zn--Cu原电池,加快反应速率
Zn和被Zn置换出的Cu、电解质溶液构成Zn--Cu原电池,加快反应速率
【解析】
(1)可根据实验设计推测实验目的,也可根据实验目的进行实验设计。分析数据可知:①②只有温度不同,①③只有浓度不同,由此可推知其实验目的;要将实验①④设计成用于探究相同温度和相同浓度的盐酸、醋酸与锌反应的反应速率,需要控制温度、浓度都相同。
(2)图中以单位时间内锌片减少的质量来表示反应速率,速率与时间成反比,结合题中所给醋酸与盐酸反应速率的关系,不难画出锌片质量与时间关系曲线。
(3)分析氯化铜加入反应体系中的变化,不难判断,使反应速率加快的原因是构成了原电池。
(1)a.实验①和②物质的温度不同,其它条件都相同,因此是探究不同温度对锌与盐酸反应速率的影响;b.实验①和③反应的温度相同,而盐酸的浓度不同,因此是探究不同浓度盐酸对锌与盐酸反应速率的影响;实验①和④是探究相同温度下,相同浓度的盐酸、醋酸与锌反应速率的区别,所以④反应温度与实验①相同,也是298K;故答案为:不同温度 不同浓度 298。
(2)实验②温度比实验①高10℃。由于反应温度每升高10℃,反应速率是原来的2倍,时间是原来的1/2,则Zn完全反应消耗的时间是10s,实验④中,温度相同、浓度相同时,醋酸的平均反应速度是盐酸的1/2,则反应时间是①的2倍,为40s.故答案用图像表示为:

(3)Zn与CuCl2溶液发生反应:Zn+CuCl2=Cu+ ZnCl2,产生的Cu与Zn及电解质溶液形成原电池,加快了反应速率。故答案为:Zn和被Zn置换出的Cu、电解质溶液构成Zn--Cu原电池,加快反应速率。

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案