题目内容
【题目】在如图所示的量热计中,将100mL![]() 溶液与
溶液与![]() 溶液混合,温度从
溶液混合,温度从![]() 升高到
升高到![]() 已知量热计的热容常数
已知量热计的热容常数![]() 量热计各部件每升高
量热计各部件每升高![]() 所需的热量
所需的热量![]() 是
是![]() 生成溶液的比热容为
生成溶液的比热容为![]() ,溶液的密度均近似为
,溶液的密度均近似为![]() .
.
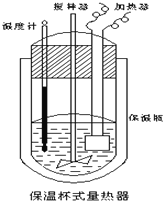
(1)试求![]() 的中和热
的中和热![]() ______.
______.
(2)![]() 的中和热的文献值为
的中和热的文献值为![]() ,则请你分析在
,则请你分析在![]() 中测得的实验值偏差可能的原因______.
中测得的实验值偏差可能的原因______.
(3)实验中NaOH过量的目的是______.
【答案】-53.3kJ/mol ①量热计的保温瓶绝热效果不好;②酸碱溶液混合不迅速;③温度计不够精确等 使碱稍稍过量,为了能保证CH3 COOH溶液完全被中和,从而提高实验的准确度
【解析】
(1)根据化学反应热的计算公式Q=-cm△T来计算;
(2)根据中和热的测定中能够导致放出的热量偏低的因素进行解答;
(3)为了确保CH3COOH溶液完全被中和,从而提高实验的准确度,所用NaOH稍过量.
![]() 温度从
温度从![]() 升高到
升高到![]() ,
,![]() ,
,![]() 的中和热
的中和热![]() ,
,
故答案为:![]() ;
;
![]() 的中和热的文献值为
的中和热的文献值为![]() ,实际上测定数值偏低,可能原因有:
,实际上测定数值偏低,可能原因有:![]() 量热计的保温瓶效果不好,
量热计的保温瓶效果不好,![]() 酸碱溶液混合不迅速,
酸碱溶液混合不迅速,![]() 温度计不够精确等,
温度计不够精确等,
故答案为:![]() 量热计的保温瓶绝热效果不好;
量热计的保温瓶绝热效果不好;![]() 酸碱溶液混合不迅速;
酸碱溶液混合不迅速;![]() 温度计不够精确等;
温度计不够精确等;
![]() 酸和碱反应测中和热时,为了保证一方全部反应,往往需要另一试剂稍稍过量,减少实验误差,所以实验中NaOH过量,为了能保证
酸和碱反应测中和热时,为了保证一方全部反应,往往需要另一试剂稍稍过量,减少实验误差,所以实验中NaOH过量,为了能保证![]() 溶液完全被中和,从而提高实验的准确度,
溶液完全被中和,从而提高实验的准确度,
故答案为:使碱稍稍过量,为了能保证![]() 溶液完全被中和,从而提高实验的准确度;
溶液完全被中和,从而提高实验的准确度;

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】市售一次性电池品种很多的,碱性锌锰电池的日常生活中用量很大。回收废旧锌锰电池并进行重新处理,可以获得MnO2及其他副产品,其工艺流程如下:
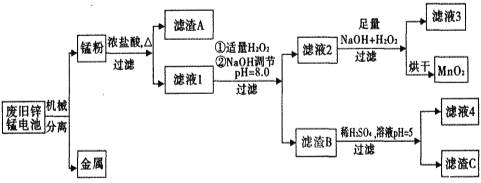
已知:“锰粉”的主要成分有MnO2、Zn(OH)2、MnOOH、碳粉,还含量有少量铁盐和亚铁盐。常温下,生成氢氧化物沉淀的pH如下表。
物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2/Mn(OH)3 |
开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
完全沉淀pH (c≤1.0x10-5mol/L) | 3.7 | 9.6 | 8.0 | 8.8 |
(1)加入NaOH溶液调节pH=8.0,目的是___。计算常温下Zn(OH)2的溶度积常数Ksp[Zn(OH)2]=___。
(2)写出滤液2中的Mn2+变成MnO2的离子方程式___。
(3)写出滤渣B与稀硫酸在pH=5时的化学方程式___。
(4)工艺中还可以将滤液4进行___、___、___、___、洗涤得到含结晶水的硫酸盐晶体。
(5)MnO2常用来制取KMnO4,在一定条件下将MnO2氧化为K2MnO4,然后用铁作阴极、铂作阳极电解K2MnO4溶液得到KMnO4。电解K2MnO4溶液的总反应方程式___。