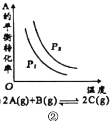
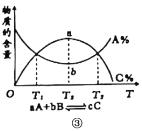
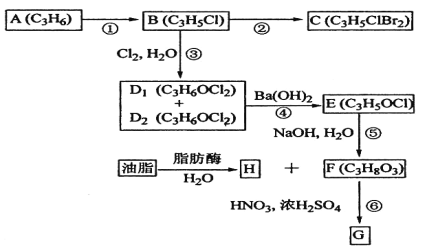
��Ŀ����
����Ŀ����84����Һ����1984�걱��ijҽԺ����ʹ�ö���������2020�꿹������״���������б��㷺��������������Ч�ɷ���NaClO��ijУ��ѧ�о���ѧϰС����ʵ�����Ʊ�NaClO��Һ������������̽���ͳɷֲⶨ��
��֪���������£�����NaClO��ҺpHΪ11
��25��ʱ��H2CO3��Ka1=4.4��10-7��Ka2=4.7��10-11��HClO��Ka=3.0��10-8
I���Ʊ�NaClO��Һ
��ѧϰС�鰴��ͼװ�ý���ʵ��(���ּг�װ��ʡȥ)
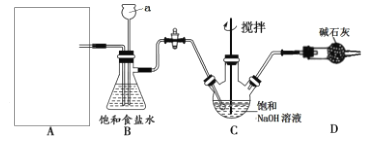
(1)��ͼ��AΪʵ�����Ʊ�Cl2�ķ���װ�ã�����ѡ������ͼ��_(�����)װ�ã��ø�װ���Ʊ�Cl2��Ӧ�Ļ�ѧ����ʽΪ__��
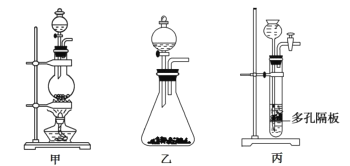
(2)Bװ��������a��������____��Bװ�ÿɳ�ȥ�������Ȼ������ʣ� �����______����(д��һ��)��
II��NaClO����̽��
����ͼװ�ý���ʵ�飬һ��ʱ���ȡCƿ�е���Һ����ʵ�飬���±���
ʵ������ | ʵ������ | |
ʵ��l | ȡ�����μ���ɫʯ����Һ | ����������ɫ |
ʵ��2 | �ⶨ��Һ��pH | 12 |
(3)Cƿ��Һ�е����ʳ�NaCl�⣬����______(�ѧʽ)��
(4)��Cƿ��NaOH��Һ����NaHCO3��Һ����Ӧһ��ʱ���ȡCƿ�е���Һ���ϱ�ʵ�����ݽ���ʵ�顣����Ϊ��ʵ��l����ɫʯ����Һ������ɫ��ʵ��2����Һ��pH=7�����ƽ���ƶ�ԭ��������ɫʯ����Һ������ɫ��ԭ����________��
III���ⶨCƿ��Һ��NaClO����(��λ��g��L-1)
i.ȡCƿ��Һ10.00mL����ƿ�У��������������ữ��Ѹ�ټ������KI��Һ���ǽ�ƿ�����ڰ�����ַ�Ӧ��
ii.��0.1000molL-1Na2S2O3����Һ�ζ�������ƿ�е���Һ���յ㣬�ظ�����2~3�Σ�����Na2S2O3��Һ��ƽ������Ϊ12.00mL��(��֪��I2+2![]() =2I-+
=2I-+![]() )
)
(5)i����Ҫ������Ӧ�����ӷ���ʽΪ_______��ii����_______��ָʾ����
(6)�ǽ�ƿ�����ڰ�����Ӧ��ԭ����________��
(7)Cƿ��Һ��NaClO������______g��L-1(����2λС��)��
���𰸡����� MnO2+4HCl(Ũ)![]() Cl2��+MnCl2+2H2O ��2KMnO4+16HCl��2KCl+2MnCl2+5Cl2��+8H2O ����©�� �������������ƽ����ѹ(��ȫƿ)������� NaClO��NaOH ��Һ�д���ƽ�� Cl2+H2OHCl+HClO��HCO3- ���� H+��ʹƽ�����ƣ�HClO Ũ������ ClO-+2I-+2H+=I2+Cl-+H2O ������Һ ��ֹHClO�ֽ�(��ֹCl2��I2�ݳ�) 4.47
Cl2��+MnCl2+2H2O ��2KMnO4+16HCl��2KCl+2MnCl2+5Cl2��+8H2O ����©�� �������������ƽ����ѹ(��ȫƿ)������� NaClO��NaOH ��Һ�д���ƽ�� Cl2+H2OHCl+HClO��HCO3- ���� H+��ʹƽ�����ƣ�HClO Ũ������ ClO-+2I-+2H+=I2+Cl-+H2O ������Һ ��ֹHClO�ֽ�(��ֹCl2��I2�ݳ�) 4.47
��������
I���Ʊ�NaClO��Һ
(1)ʵ�����Ʊ�Cl2�����ö���������Ũ������ȵķ��������ݷ�Ӧ�������װ�ÿ�֪�Һͱ����ܽ��м��ȣ�ֻ���ڼ�װ���н��з�Ӧ��������Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl(Ũ)![]() Cl2��+MnCl2+2H2O�������ò��ø��������Ũ���᳣�����Ʊ�����������Ҫ����װ�ã�ͬʱ��������������ˮ����ѡ�ñ�װ����ȡ��Ӧ������װ���н��У�������Ӧ�Ļ�ѧ����ʽΪ��2KMnO4+16HCl��2KCl+2MnCl2+5Cl2��+8H2O��
Cl2��+MnCl2+2H2O�������ò��ø��������Ũ���᳣�����Ʊ�����������Ҫ����װ�ã�ͬʱ��������������ˮ����ѡ�ñ�װ����ȡ��Ӧ������װ���н��У�������Ӧ�Ļ�ѧ����ʽΪ��2KMnO4+16HCl��2KCl+2MnCl2+5Cl2��+8H2O��
�ʴ�Ϊ�����ң�MnO2+4HCl(Ũ)![]() Cl2��+MnCl2+2H2O��2KMnO4+16HCl��2KCl+2MnCl2+5Cl2��+8H2O��
Cl2��+MnCl2+2H2O��2KMnO4+16HCl��2KCl+2MnCl2+5Cl2��+8H2O��
(2) Bװ��������aΪ����©����Bװ�ÿɳ�ȥ�������Ȼ������ʣ� ������©���������ͨ��������ƽ������ѹǿ�����ôӶ�����Ч�ķ�ֹ���������������������������������B�У�
�ʴ�Ϊ������©�����������������ƽ����ѹ(��ȫƿ)���������
II��NaClO����̽��
(3) Cƿ��Һ�е����ʳ�NaCl�⣬�����ڲ���������ƣ��������£�����NaClO��ҺpHΪ11��C����Һ��pHֵ12���Ӷ�˵����Һ������δ��Ӧ����������ƣ�
�ʴ�Ϊ��NaClO��NaOH��
(4) ��Һ�д���ƽ��Cl2+H2OHCl+HClO�����̼������Ա�������������H2CO3��Ka1=4.4��10-7��HClO��Ka=3.0��10-8����֪̼������ǿ�ڴ����ᣬ��̼������ֻ�����ᷴӦ����������ᷴӦ��HCO3- ����H+��ʹƽ�����ƣ�HClO Ũ������HClOŨ��Խ��Ư��������ǿ�����ʹ��ɫʯ����ɫ��
�ʴ�Ϊ����Һ�д���ƽ��Cl2+H2OHCl+HClO��HCO3- ����H+��ʹƽ�����ƣ�HClO Ũ������
III���ⶨCƿ��Һ��NaClO����(��λ��g��L-1)
(5)i.ȡCƿ��Һ10.00mL����ƿ�У��������������ữ��Ѹ�ټ������KI��Һ��C�е�ClO-����ǿ�����������������ӣ�������Ӧ�����ӷ���ʽΪ��ClO-+2I-+2H+=I2+Cl-+H2O��ii.��0.1000molL-1Na2S2O3����Һ�ζ����ⵥ�ʵ���Һ���յ㣬Ӧѡ�õ�����ָʾ����
�ʴ�Ϊ��ClO-+2I-+2H+=I2+Cl-+H2O�����ۣ�
(6) �ǽ�ƿ�����ڰ�����Ӧ����Ҫԭ���ǣ�HClO���ȶ��������Ȼ����������������ֽⷴӦ��ͬʱҲ���Է�ֹ��Һ�в����������͵��ݳ����ʴ�Ϊ����ֹHClO�ֽ�(��ֹCl2��I2�ݳ�)
(7) ��Ϸ�ӦClO-+2I-+2H+=I2+Cl-+H2O��I2+2![]() =2I-+
=2I-+![]() ������ת����ϵ��֪
������ת����ϵ��֪![]() ����
����![]() ��Cƿ��Һ��NaClO������
��Cƿ��Һ��NaClO��������
�ʴ�Ϊ��4.47��

����Ŀ����ʵ�����װ��С�ɡ���ԼҩƷ��������㡢�������ԡ���ȫ�ɿ���������Ⱦ���ŵ㣬��ͼ��ijͬѧ��Ƶ�ʵ������ȡCl2��̽���仯ѧ���ʵ���װ��(ͼ�мг�װ�þ���ȥ)��
�������ϣ������������Դ���HIO3��
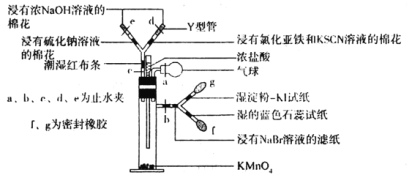
�ش��������⣺
(1)ʵ�����пɴ���ͼ������Ũ���������������___________��
(2)����Ũ������Թ��ڷ�����Ӧ�Ļ�ѧ����ʽ��__________________________________��
(3)̽�������Ļ�ѧ���ʣ���ʵ��������д���±���Ӧ�Ŀո��___________
�������� | ʵ������ |
��������Ũ���ᣬ��c��d��e��ʹ������������������Y�Թ� | |
�ر�c��b��ʹ������������Y���� |
(4)ʵ���з�����������ͨ�������࣬���۵⻯����ֽ����Ϊ��ɫ�����ܵ�ԭ����__________________________________________________��
(5)��װ��___________(��ܡ����ܡ�)֤��������˳��Cl2>Br2>I2��ԭ����___________��ʵ����Ϻر�ֹˮ��b����a��c����ѹ����Ŀ����__________________________��