题目内容
【题目】(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。
①在提纯时为了除去Fe2+,常加入合适的氧化剂,使Fe2+转化为Fe3+,下列物质可作氧化剂的是__(填字母)。
A.KMnO4 B.H2O2 C.氯水 D.HNO3
②然后再加入适当物质调整溶液pH至4,使Fe3+转化为Fe(OH)3,调整溶液pH可选用___(填字母)。
A.NaOH B.NH3·H2O C.CuO D.Cu(OH)2
(2)甲同学怀疑调整溶液pH至4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=1.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常残留在溶液中的离子浓度小于1.0×10-5mol·L-1时就被认定为沉淀完全,设溶液中CuSO4的浓度为3.0mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为__,Fe3+完全沉淀[即c(Fe3+)≤1.0×10-5mol·L-1]时溶液的pH为__,通过计算确定上述方案__(填“可行”或“不可行”)。
【答案】B CD 4 3 可行
【解析】
(1)加入合适的氧化剂,使Fe2+氧化为Fe3+,需要不能引入新的杂质;调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,则加含铜元素的物质与氢离子反应促进铁离子水解转化为沉淀;
(2)依据氢氧化铜饱和溶液中溶度积常数计算溶液中的氢离子浓度计算Cu(OH)2开始沉淀时溶液的pH;结合氢氧化铁溶度积和残留在溶液中的离子浓度小于1×10-5molL-1时就认为沉淀完全,计算Fe(OH)3沉淀完全时的pH。
(1)①加入合适的氧化剂,使Fe2+氧化为Fe3+,但不能引入新的杂质,A、C、D中会引入杂质,只有过氧化氢的还原产物为水,不引入杂质,故只有B符合,故答案为:B;
②调整溶液至pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,则加含铜元素的物质与氢离子反应促进铁离子水解转化为沉淀,则C、D均可,A、B能够将铜离子也转化为沉淀,不符合,故答案为:CD;
(2)Cu(OH)2的溶度积Ksp=3.0×10-20,溶液中CuSO4的浓度为3.0molL-1,c(Cu2+)=3.0molL-1,依据溶度积常数c(Cu2+)×c2(OH-)=3.0×10-20;c2(OH-)=![]() =10-20;得到c(OH-)=10-10mol/L,依据水溶液中的离子积c(H+)×c(OH-)=10-14,则c(H+)=10-4mol/L,溶液pH=4,则Cu(OH)2开始沉淀时溶液的pH为4;残留在溶液中的离子浓度小于1×10-5molL-1时就认为沉淀完全,Fe(OH)3的溶度积Ksp=1.0×10-38,c(Fe3+)×c3(OH-)=1.0×10-38;c3(OH-)=
=10-20;得到c(OH-)=10-10mol/L,依据水溶液中的离子积c(H+)×c(OH-)=10-14,则c(H+)=10-4mol/L,溶液pH=4,则Cu(OH)2开始沉淀时溶液的pH为4;残留在溶液中的离子浓度小于1×10-5molL-1时就认为沉淀完全,Fe(OH)3的溶度积Ksp=1.0×10-38,c(Fe3+)×c3(OH-)=1.0×10-38;c3(OH-)=![]() =1.0×10-33,则c(OH-)=1×10-11mol/L;水溶液中的离子积c(H+)×c(OH-)=10-14;c(H+)=1×10-3mol/L,则pH=3;通过计算可知pH=4能达到除去Fe3+而不损失Cu2+的目的,则方案可行,故答案为:4;3;可行。
=1.0×10-33,则c(OH-)=1×10-11mol/L;水溶液中的离子积c(H+)×c(OH-)=10-14;c(H+)=1×10-3mol/L,则pH=3;通过计算可知pH=4能达到除去Fe3+而不损失Cu2+的目的,则方案可行,故答案为:4;3;可行。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某强酸性无色溶液中可能含下表离子中的若干种离子。
阳离子 | Mg2+、NH4+、Ba2+、Al3+、Fe2+ |
阴离子 | SiO32-、MnO4-、Cl-、NO3-、SO42- |
实验Ⅰ:取少量该强酸性溶液A进行如下实验。
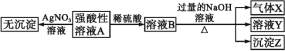
实验Ⅱ:为了进一步确定该溶液的组成,取100 mL原溶液A,向该溶液中滴加1 mol·L-1的NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。
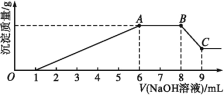
回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有________种。
(2)通过实验Ⅰ可以确定该溶液中一定存在的阴离子是_________。检验气体X的方法是_______________;沉淀Z的化学式为_____________。
(3)写出实验Ⅱ的图示中BC段对应反应的离子方程式:________________。
(4)A点对应的固体质量为____ g。
(5)通过上述信息,推算该溶液中阴离子的浓度为________ mol·L-1。