题目内容
18.某NaHCO3样品中含有NaCl杂质,为测定试样中NaHCO3的质量分数,某同学设计了二种方案:Ⅰ、方案一:称取10g样品按如图1装置进行测定.
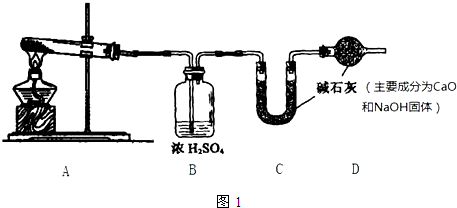
(1)装置A中反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(2)装置D的作用是吸收空气中的水和二氧化碳.
(3)完全反应时,若测得C装置在反应前后的质量差是2.0g,则样品中NaHCO3的质量分数为76.4%.
(4)此方案的实验结果数值偏小,可能的原因是CO2残留于AB装置中.
Ⅱ、方案二:取4g样品溶于水,加入适当指示剂,逐滴滴入1mol/L硫酸,待恰好完全反应时,测定所消耗的硫酸的体积.
回答下列问题:
(1)上述测定,需用已知浓度的浓硫酸配制100mL 1mol/L的稀硫酸;
①配制过程中不需要用到的仪器是图2中的D.
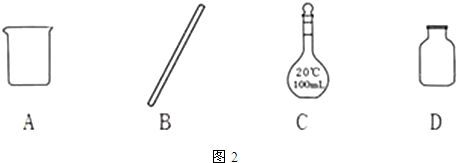
②配制过程中出现以下情况,对所配制溶液浓度无影响的是C.
A.没有洗涤烧杯和玻璃棒.
B.如果加水超过了刻度线,取出水使液面恰好到刻度线.
C.容量瓶没有干燥.
(2)滴加硫酸时反应的化学方程式是2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑.
(3)恰好完全反应时,若测得消耗硫酸的体积为20mL,则样品中NaHCO3的质量分数为84%.
分析 方案一:根据装置图可知,碳酸氢钠在A中受热分解,生成二氧化碳和水蒸汽,混合气体通过浓硫酸吸水,根据浓硫酸的质量变化判断生成水的质量,再能过U形管中的碱石灰,吸收生成的二氧化碳,根据固体的质量的变化得出二氧化碳的质量,装置最后的干燥管中碱石灰可以防止空气中的水和二氧化碳对实验数据的干扰;
方案二:用碳酸氢钠与硫酸反应,依据滴定过程硫酸和碳酸氢钠反应的定量关系计算纯碳酸氢钠的质量,再根据$\frac{NaHC{O}_{3}的质量}{样品的质量}$×100%计算样品中NaHCO3的质量分数,根据配制一定物质的量的浓度溶液的实验要求,确定需要的仪器,根据实验操作中对$c=\frac{{n}_{B}}{{V}_{溶液}}$中的nB和V溶液的影响判断对溶液浓度的影响,据此答题.
解答 解:Ⅰ、方案一:根据装置图可知,碳酸氢钠在A中受热分解,生成二氧化碳和水蒸汽,混合气体通过浓硫酸吸水,根据浓硫酸的质量变化判断生成水的质量,再能过U形管中的碱石灰,吸收生成的二氧化碳,根据固体的质量的变化得出二氧化碳的质量,装置最后的干燥管中碱石灰可以防止空气中的水和二氧化碳对实验数据的干扰,
(1)碳酸氢钠在A中受热分解,生成二氧化碳和水蒸汽,反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(2)根据上面的分析可知,装置D的作用是吸收空气中的水和二氧化碳,
故答案为:吸收空气中的水和二氧化碳;
(3)完全反应时,若测得C装置在反应前后的质量差是2.0g,即生成的二氧化碳的质量为2.0g,设NaHCO3的质量为m,
根据方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
84×2 44
m 2.0g
所以m=$\frac{84×2×2}{44}$g=7.64g
样品中NaHCO3的质量分数为$\frac{7.64g}{10g}$×100%=76.4%,
故答案为:76.4%;
(4)此方案的实验结果数值偏小,可能的原因是CO2残留于AB装置中,未能在C中测出,
故答案为:CO2残留于AB装置中;
Ⅱ、方案二:用碳酸氢钠与硫酸反应,依据滴定过程硫酸和碳酸氢钠反应的定量关系计算纯碳酸氢钠的质量,再根据$\frac{NaHC{O}_{3}的质量}{样品的质量}$×100%计算样品中NaHCO3的质量分数,根据配制一定物质的量的浓度溶液的实验要求,确定需要的仪器,根据实验操作中对$c=\frac{{n}_{B}}{{V}_{溶液}}$中的nB和V溶液的影响判断对溶液浓度的影响,
(1)①配制过程中需要用到烧杯、玻璃棒、容量瓶,不用集气瓶,
故选D;
②A、没有洗涤烧杯或玻璃棒,导致配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,
B、如果加水超过了刻度线,取出水使液面恰好到刻度线,溶液浓度减小;
C、容量瓶洗净后没有干燥,对溶质的物质的量及最终溶液的体积都没有影响,所以不影响配制结果,
故答案为:C;
(2)滴加硫酸时反应的化学方程式是2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑,
故答案为:2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑;
(3)若测得消耗硫酸的体积为20mL,硫酸浓度为1mol/L
2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑
2 1
n 1mol/L×0.02L
n=0.04mol
样品中NaHCO3的质量分数=$\frac{0.04mol×84g/mol}{4g}$×100%=84%;
故答案为:84%.
点评 本题考查了物质组成的实验探究和分析判断,主要是实验基本操作和定量计算应用,掌握基础是解题关键,题目难度中等.

 |  | 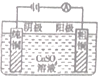 |  | |
| 化工 | 氯碱工业 | 高炉炼铁 | 铜的精炼 | 生产漂白粉 |
| 原理 | 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$ 2NaOH+Cl2↑+ H2↑ | 3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | 阴极: Cu2++2e-═Cu | 2NaOH+Cl2═NaCl+NaClO+H2O |
| A | B | C | D |
| A. | A | B. | B | C. | C | D. | D |
| A. | 化学反应不一定有分子碰撞 | B. | 化学反应的活化能一定大于零 | ||
| C. | 具有较高能量的分子是活化分子 | D. | 发生有效碰撞的分子是活化分子 |
| 元素 | 元素性质或结构 |
| A | 最外层电子数是其内层电子数的2倍 |
| B | B元素的单质在空气中含量最多 |
| C | C元素在地壳中含量最多 |
| D | D元素在同周期中金属性最强 |
| E | 常温常压下,E元素形成的单质是淡黄色固体,常在火山口附近沉积 |
(2)B最简单气态氢化物的电子式
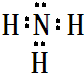 ,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式
,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式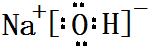 ,所含化学键类型:离子键、共价键.
,所含化学键类型:离子键、共价键.(3)B、C、D、E简单离子半径由大到小顺序为:S2->N3->O2->Na+(填元素符号).
(4)用电子式表示E的氢化物的形成过程
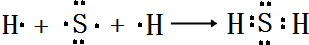 .
.(5)由A、B、C与氢元素组成的一种常见酸式盐与过量D的最高价氧化物的水化物反应的离子方程式:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O.
(6)19.2g金属铜与一定浓度的B的最高价氧化物的水化物反应,产生标准状况下NO、NO2(不考虑N2O4的存在)混合气6.72L,则参加反应的HNO3的物质的量为0.9mol.
| A. | 1.6a g | B. | (a-1.6)g | C. | (a-3.2)g | D. | 无法计算 |
| A. | 根瘤菌把氮气转化为氨 | B. | 氮气和氢气在适宜条件下合成氨 | ||
| C. | 氮气和氧气在放电条件下合成NO | D. | 工业上用氨和二氧化碳合成尿素 |

下列说法中不正确的是( )
| A. | 该过程是一种新的硫酸生产方法 | |
| B. | C2H5OSO3H具有酸性 | |
| C. | 该过程中①、②是加成反应 | |
| D. | 该过程中③、④可看做酯类的水解反应 |