��Ŀ����
(14��) ��Դ��ȱ������������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��1����ҵ��һ������������ַ�Ӧ�ϳɼ״���
��ӦI�� CO(g) �� 2H2(g) CH3OH(g)
CH3OH(g)
��ӦII�� CO2(g) �� 3H2(g) CH3OH(g) + H2O(g)
CH3OH(g) + H2O(g)
������Ӧ���ϡ�ԭ�Ӿ��á�ԭ����� ���I������
��2����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l) �� 3O2(g) �� 2CO2(g) �� 4H2O(g) ��H ����1275.6 kJ��mol
�� 2CO (g)+ O2(g) �� 2CO2(g) ��H ����566.0 kJ��mol
�� H2O(g) �� H2O(l) ��H ����44.0 kJ��mol
��CH3OH(l)+ O2(g) �� CO(g) + 2H2O(l) ��H��
��3��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ�������������ͼ��ʾ�ĵ��װ�á�
�� �õ�ظ����ĵ缫��ӦΪ ��
�� ����һ��ʱ������Һ��pH ���������䡢��С����
���øõ������Դ�����������ͼ��ʾװ��(a��b��c��d��Ϊʯī�缫)��������װ250mL0.04mol/LCuSO4��Һ��������װ300mL����NaCl��Һ��д��c�缫�ĵ缫��Ӧ �������£���300mL����Һ��pHΪ13ʱ���Ͽ���Դ�����ڼ״����������O2�����Ϊ mL(��״��) ����������м�����������ijһ�����ʣ�����ʹ��Һ�ָ���ԭ��״̬���������� (��д���) ��

��1����ҵ��һ������������ַ�Ӧ�ϳɼ״���
��ӦI�� CO(g) �� 2H2(g)
 CH3OH(g)
CH3OH(g) ��ӦII�� CO2(g) �� 3H2(g)
 CH3OH(g) + H2O(g)
CH3OH(g) + H2O(g) ������Ӧ���ϡ�ԭ�Ӿ��á�ԭ����� ���I������
��2����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l) �� 3O2(g) �� 2CO2(g) �� 4H2O(g) ��H ����1275.6 kJ��mol
�� 2CO (g)+ O2(g) �� 2CO2(g) ��H ����566.0 kJ��mol
�� H2O(g) �� H2O(l) ��H ����44.0 kJ��mol
��CH3OH(l)+ O2(g) �� CO(g) + 2H2O(l) ��H��
��3��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ�������������ͼ��ʾ�ĵ��װ�á�
�� �õ�ظ����ĵ缫��ӦΪ ��
�� ����һ��ʱ������Һ��pH ���������䡢��С����
���øõ������Դ�����������ͼ��ʾװ��(a��b��c��d��Ϊʯī�缫)��������װ250mL0.04mol/LCuSO4��Һ��������װ300mL����NaCl��Һ��д��c�缫�ĵ缫��Ӧ �������£���300mL����Һ��pHΪ13ʱ���Ͽ���Դ�����ڼ״����������O2�����Ϊ mL(��״��) ����������м�����������ijһ�����ʣ�����ʹ��Һ�ָ���ԭ��״̬���������� (��д���) ��
| A��CuO | B��CuCO3���� | C��Cu(OH)2 | D��Cu2(OH)2CO3 |

��1�� I ��2�֣���2�� ��H����442.8 kJ�Mmol��2�֣�
��3����CH3OH + 8OH- = CO32- + 6H2O + 6e-��2�֣�
�ڼ�С��2�֣��� 2Cl- - 2e-=Cl2�� ��2�֣�168��2�֣� D��2�֣�
�����������1����ӦIԭ��������100%������ԭ�Ӿ��ã���2��CH3OH(l)+ O2(g) �� CO(g) + 2H2O(l)
��H����H1����H2 ��2��H3 = ��442.8 kJ�Mmol����3�����Խ����£��״�ʧȥ��������CO32-��CH3OH + 8OH- = CO32- + 6H2O + 6e-��CH3OH + 8OH-�� 6e- = CO32- + 6H2O���ڷ�Ӧ���ܷ���ʽΪ2CH3OH + 4OH- + 3O2 = 2CO32- + 6H2O������һ��ʱ�����Һ��pH���٣��۵�ⱥ��ʳ��ˮ����ʽΪ
2NaCl+2H2O=" 2NaOH" + H2+ Cl2����Ӧ������n(OH-)="0.3��0.1=0.03mol=" n(e-)��v(O2)=0.03��4��22.4��1000=168mL�����������������������������Ȳ���ͭ0.01mol�����������0.005mol���ʼ���Cu2(OH)2CO3���ָܻ�ԭ��״̬��

��ϰ��ϵ�д�
 ����ʦ���һ��һ��ϵ�д�
����ʦ���һ��һ��ϵ�д�
�����Ŀ
 [Cu��NH3��3]Ac?CO��aq������H��0��
[Cu��NH3��3]Ac?CO��aq������H��0��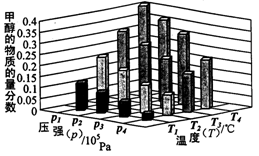
 ��
�� ��ʵ����N��N������Ϊ167kJ��mol��1�� NO2�е�������ƽ������Ϊ466 kJ��mol��1��N2O4�е�������ƽ������Ϊ438.5 kJ��mol��1��
��ʵ����N��N������Ϊ167kJ��mol��1�� NO2�е�������ƽ������Ϊ466 kJ��mol��1��N2O4�е�������ƽ������Ϊ438.5 kJ��mol��1�� 2NO2(g)�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����
2NO2(g)�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ���� 
 N2O4��ƽ�ⳣ��K�� �����������С�����䡱����
N2O4��ƽ�ⳣ��K�� �����������С�����䡱���� 2NO(g) ��H����֪�÷�Ӧ�� T ��ʱ��ƽ�ⳣ��K��9.0��
2NO(g) ��H����֪�÷�Ӧ�� T ��ʱ��ƽ�ⳣ��K��9.0��


 mol;
mol;

 ���>������<����=����
���>������<����=���� 3N2��2X��4H2O
3N2��2X��4H2O