题目内容
【题目】I.新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
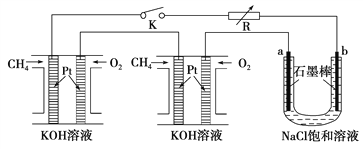
回答下列问题:
(1)甲烷燃料电池负极的电极反应式为________________________。
(2)闭合开关K后,a、b电极上均有气体产生,其中b电极上得到的是________,电解氯化钠溶液的总反应离子方程式为__________________________。
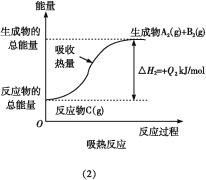
II.用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示。(电极材料为石墨)

(1)图中a极要连接电源的(填“正”或“负”)________极,C口流出的物质是________。
(2)b电极SO![]() 放电的电极反应式为____________。
放电的电极反应式为____________。
(3)电解过程中阴极区碱性明显增强,用平衡移动原理解释原因________________。
【答案】 ) CH4-8e-+10OH-===CO![]() +7H2O H2 2Cl-+2H2O
+7H2O H2 2Cl-+2H2O![]() Cl2↑+H2↑+2OH- 负 硫酸 SO
Cl2↑+H2↑+2OH- 负 硫酸 SO![]() -2e-+H2O===SO
-2e-+H2O===SO![]() +2H+ H2O
+2H+ H2O![]() H++OH-,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强
H++OH-,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强
【解析】I.(1)甲烷燃料电池负极的电极反应式为CH4-8e-+10OH-===CO![]() +7H2O。
+7H2O。
(2)闭合开关K后,a、b电极上均有气体产生,其中b电极为阴极,氢离子在阴极上放电得到的H2,电解氯化钠溶液的总反应离子方程式为2Cl-+2H2O![]() Cl2↑+H2↑+2OH-。
Cl2↑+H2↑+2OH-。
II.由图中信息可知,电解池左室为阴极室、右室为阳极室,所以a、b分别为电源的负极和正极。在阴极通入稀氢氧化钠溶液,电解生成氢气和氢氧化钠;在阳极通入稀硫酸,亚硫酸根通过阴离子交换膜进入阳极室放电生成硫酸。
(1)图中a极要连接电源的负极,C口流出的物质是硫酸。
(2)b电极SO![]() 放电的电极反应式为SO
放电的电极反应式为SO![]() -2e-+H2O===SO
-2e-+H2O===SO![]() +2H+。
+2H+。
(3)电解过程中阴极区碱性明显增强,是因为水有电离平衡H2O![]() H++OH-存在,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强。
H++OH-存在,在阴极H+放电生成H2,c(H+)减小,水的电离平衡正向移动,碱性增强。

 每课必练系列答案
每课必练系列答案【题目】根据表中信息,判断下列叙述中正确的是
序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
① | Cl2 | FeBr2 | / | Cl- | |
② | KClO3 | 浓盐酸 | / | Cl2 | |
③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O