题目内容
15.(1)为降低硫的氧化物对空气的污染,可把氧化钙和含硫的煤混和后燃烧,这种方法叫做钙基固硫,试写出有关的化学方程式CaO+SO2=CaSO3、2CaSO3+O2=2CaSO4.(2)火力发电站废气中含有SO2.为除去有害气体SO2,可用碳酸钙或氢氧化钙的悬浊
洗涤,反应产物为CaSO4,写出上述两种途径有关的化学方程式.
①2SO2+O2+2CaCO3═2CaSO4+2CO2
②2SO2+O2+2Ca(OH)2=2CaSO4+2CO2+2H2O
试说明用熟石灰的悬浊液,而不用澄清石灰水洗涤废气的理由熟石灰悬浊液吸收SO2速度快且脱硫率高.澄清石灰水中Ca(OH)2浓度较小,吸收SO2的量少;熟石灰固体与气体接触面小吸收速度慢且脱硫率低.
分析 (1)二氧化硫与氧化钙反应生成亚硫酸钙,亚硫酸钙与氧气反应生成硫酸钙;
(2)①二氧化硫与碳酸钙、氧气反应生成硫酸钙、二氧化碳;
②二氧化硫与氢氧化钙、氧气反应生成硫酸钙和水;
氢氧化钙的溶解度较小,吸收SO2的量少.
解答 解:(1)二氧化硫与氧化钙反应生成亚硫酸钙方程式:CaO+SO2=CaSO3,亚硫酸钙与氧气反应生成硫酸钙:2CaSO3+O2=2CaSO4;
故答案为:CaO+SO2=CaSO3;2CaSO3+O2=2CaSO4;
(2)①二氧化硫与碳酸钙、氧气反应生成硫酸钙、二氧化碳,方程式:2SO2+O2+2CaCO3═2CaSO4+2CO2;
故答案为:2SO2+O2+2CaCO3═2CaSO4+2CO2;
②二氧化硫与氢氧化钙、氧气反应生成硫酸钙和水,化学方程式:2SO2+O2+2Ca(OH)2=2CaSO4+2H2O;
故答案为:2SO2+O2+2Ca(OH)2=2CaSO4+2H2O;
因为氢氧化钙的溶解度较小,得到的澄清石灰水的浓度较小,吸收SO2的量少,所以熟石灰悬浊液吸收SO2速度快且脱硫率高.熟石灰固体与气体接触面小吸收速度慢且脱硫率低,所以不用澄清石灰水或熟石灰的固体吸收二氧化硫,
故答案为:熟石灰悬浊液吸收SO2速度快且脱硫率高.澄清石灰水中Ca(OH)2浓度较小,吸收SO2的量少;熟石灰固体与气体接触面小吸收速度慢且脱硫率低.
点评 本题考查了工业脱硫的原理,侧重化学方程式的书写,明确二氧化硫的还原性是解题关键,为高考频考题,注意对相关知识的积累,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.8NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA | |
| D. | 含4molHCl的浓盐酸与足量的二氧化锰在加热条件下反应,一定能产生NA个Cl2气体分子 |
20.某元素M2+核外电子数为24,该元素是下列原子中的( )
| A. | ${\;}_{24}^{52}$Cr | B. | ${\;}_{12}^{24}$Mg | C. | ${\;}_{26}^{56}$Fe | D. | ${\;}_{22}^{48}$Ti |
4.下列实验设计及其对应的离子方程式均正确的是( )
| A. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| B. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O═C6H5OH+HSO3- | |
| C. | 向海带灰浸出液中加入稀硫酸、双氧水:2I-+2H++H2O2═I2+2H2O | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
5.利用下列实验装置能完成相应实验的是( )
| A. |  用于证明非金属性强弱:Cl>C>Si | B. | 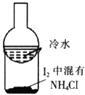 用于分离I2和NH4Cl | ||
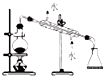
| C. |  装置能组成Zn、Cu原电池 | D. |  用于测定某稀盐酸的物质的量浓度 |




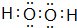 ;
;