题目内容
5.铁酸钠是水处理过程中使用的一种新型净水剂.铁酸钠之所以能净水,是因为该 物质既能消毒杀菌、其反应后的产物又能吸附杂质.制取铁酸钠(M)的化学方程式为:2FeNO3+16NaOH+3CI2═2M+6NaNO3+6NaCI+8H2O.则M的化学式是( )| A. | NaFeO4 | B. | Na2FeO4 | C. | NaFe2O4 | D. | Na2Fe3O8 |
分析 根据反应的化学方程式2Fe(NO3)3+16NaOH+3Cl2=2M+6NaNO3+6NaCl+8H2O,利用质量守恒定律来推断M的化学式.
解答 解:在反应2Fe(NO3)3+16NaOH+3Cl2=2M+6NaNO3+6NaCl+8H2O中,根据质量守恒定律可知,元素的种类和原子个数在反应前后不变,N、H、Cl元素的原子在反应前后的个数相等,反应前共2个Fe,则M中应有2个Fe,反应前共16个Na原子,反应后现有12个Na原子,则M中应有4个Na原子,反应前共34个O原子,反应后现有26个O原子,则M中应有8个O原子,又M的化学计量数为2,则M的化学式为Na2FeO4,
故选B.
点评 本题考查学生利用化学方程式来推断物质的化学式,学生应能利用元素守恒和原子守恒来得出物质中的原子个数,结合化学计量数得出化学式.

练习册系列答案
相关题目
15.从元素化合价变化的角度分析,下列反应中,画线的物质发生氧化反应的是( )
| A. | SO2+2NaOH═Na2SO3+H2O | |
| B. | 2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | |
| C. | 2FeCl3+Fe═3FeCl2 | |
| D. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ |
20.体积为1L的干燥容器中充入一定量HCl气体后,测得容器中气体对氧气的相对密度为1.082.则容器中HCl气体的质量分数约为( )
| A. | 75% | B. | 25% | C. | 79.1% | D. | 78.1% |
17.下图分别表示四种操作,其中有两处错误的是( )
| A. | 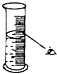 读数 | B. |  稀释 | C. | 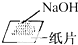 称量 | D. | 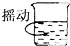 溶解 |
15. 如图为美国布朗大学的科学家使用硅碲化物制造出的新型纳米颗粒材料,可广泛应用于电子和光学设备中.将该纳米颗粒分散到水中,下列有关该分散系的说法中正确的是( )
如图为美国布朗大学的科学家使用硅碲化物制造出的新型纳米颗粒材料,可广泛应用于电子和光学设备中.将该纳米颗粒分散到水中,下列有关该分散系的说法中正确的是( )
 如图为美国布朗大学的科学家使用硅碲化物制造出的新型纳米颗粒材料,可广泛应用于电子和光学设备中.将该纳米颗粒分散到水中,下列有关该分散系的说法中正确的是( )
如图为美国布朗大学的科学家使用硅碲化物制造出的新型纳米颗粒材料,可广泛应用于电子和光学设备中.将该纳米颗粒分散到水中,下列有关该分散系的说法中正确的是( )| A. | 该分散系属于溶液 | B. | 该分散系能产生丁达尔效应 | ||
| C. | 该分散系不能通过滤纸 | D. | 该分散系的隐定性强于食盐水 |

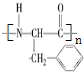 (写结构简式);
(写结构简式); ;
;