题目内容
9.已知:C(s)+H2O (g)=CO(g)+H2(g)△H=+130kJ•mol-12C(s)+O2(g)=2CO(g)△H=-220kJ•mol-1
H-H、O-H和O=O键的键能分别为436、462和akJ•mol-1,则a为( )
| A. | 1352 | B. | 1456 | C. | 496 | D. | 360 |
分析 根据盖斯定律①C(s)+H2O(g)═CO(g)+H2(g)△H=+130kJ•mol-1,
②2C(s)+O2(g)═2CO(g)△H=-220kJ•mol-1
①×2-②计算水分解反应的焓变,化学反应的焓变△H=H产物-H反应物再结合化学键能和物质能量的关系来回答.
解答 解:O=O键的键能为aJ•mol-1,
已知①C(s)+H2O(g)═CO(g)+H2(g)△H=+130kJ•mol-1,
②2C(s)+O2(g)═2CO(g)△H=-220kJ•mol-1
①×2-②得:2H2O(g)═O2(g)+2H2(g)△H=480kJ•mol-1,
△H=4×462-a-2×436=480kJ•mol-1,
解得a=496 kJ•mol-1,
故选C.
点评 本题考查学生盖斯定律的应用以及化学反应的能量和化学键键能之间的关系,注意知识的迁移和应用是关键,难度中等.

练习册系列答案
相关题目
19.下表是某地区市场上销售的一种“加碘食盐”的包装袋上的部分文字说明.请根据下表回答下列问题.
①碘是合成下列哪种激素的主要原料之一B.
A.胰岛素 B.甲状腺素
C.生长激素 D.雄性激素
②长期生活在缺碘山区,又得不到食盐的供应,易患C.
A.甲状腺亢进 B.贫血症
C.地方性甲状腺肿大 D.糖尿病
③食盐中加碘,这碘指的是元素(填“元素”、“原子”或“单质”).
④碘酸钾的化学式为KIO3,其中碘元素的化合价为+5.
| 配料表 | 精制海盐、碘酸钾 |
| 含碘量 | 20mg/kg~40mg/kg |
| 储存方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
A.胰岛素 B.甲状腺素
C.生长激素 D.雄性激素
②长期生活在缺碘山区,又得不到食盐的供应,易患C.
A.甲状腺亢进 B.贫血症
C.地方性甲状腺肿大 D.糖尿病
③食盐中加碘,这碘指的是元素(填“元素”、“原子”或“单质”).
④碘酸钾的化学式为KIO3,其中碘元素的化合价为+5.
20.从溴乙烷制取1,2-二溴乙烷,下列转化方案中最好的是( )
| A. | CH3CH2Br$→_{△}^{NaOH水溶液}$CH3CHOH$→_{170℃}^{浓H_{2}SO_{4}}$CH2═CH2$\stackrel{Br}{→}$CH2BrCH2Br | |
| B. | CH3CH2Br$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| C. | CH3CH2Br$→_{醇溶液}^{NaOH}$CH2═CH2$\stackrel{HBr}{→}$CH2BrCH3$\stackrel{Br}{→}$CH2BrCH2Br | |
| D. | CH2BrCH2Br$\stackrel{NaOH醇溶液}{→}$CH2═CH2$\stackrel{Br}{→}$CH2BrCH2Br |
17.用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.用相同浓度和体积的氨水(NH3•H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会( )
| A. | 偏大 | B. | 偏小 | C. | 无影响 |
4.根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
| A. | 铍原子失电子的能力比钙弱 | B. | 砹的氢化物不如碘化氢稳定 | ||
| C. | 硒酸的酸性比硫酸强 | D. | 氢氧化锶的碱性比氢氧化钙强 |
1.已知H2(g)+Cl2(g)=2HCl(g)△H=-184.6kJ•mol-1,则反应HCl(g)=$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)的△H为( )
| A. | +184.6 kJ•mol-1 | B. | -92.3 kJ•mol-1 | C. | +92.3 kJ•mol-1 | D. | +92.3kJ |
18.下列不能加快化学反应速率的是( )
| A. | 升高温度 | B. | 增大反应物浓度 | C. | 降低温度 | D. | 加入催化剂 |
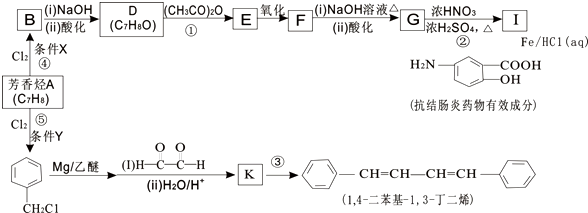
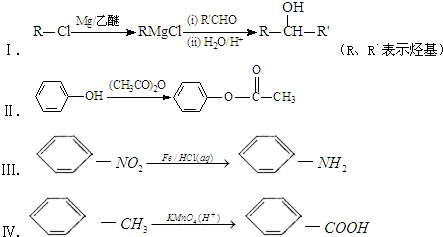
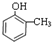
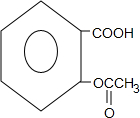 +3NaOH→
+3NaOH→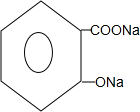 +CH3COONa+2H2O.
+CH3COONa+2H2O. 有氯原子的方法是将少量样品与NaOH溶液在试管中混合共热,充分反应并冷却后,向溶液中加稀HNO3酸化,再滴加AgNO3溶液,若有白色白色沉淀,则证明有氯元素.
有氯原子的方法是将少量样品与NaOH溶液在试管中混合共热,充分反应并冷却后,向溶液中加稀HNO3酸化,再滴加AgNO3溶液,若有白色白色沉淀,则证明有氯元素. .
.
 溶液中的离子反应
溶液中的离子反应