题目内容
【题目】下列表示不正确的是( )
A. 氯离子的结构示意图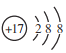 B. 四氯化碳分子的电子式:
B. 四氯化碳分子的电子式: 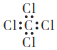
C. CH4的球棍模型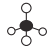 D. 明矾的化学式:KAl(SO4)2·12H2O
D. 明矾的化学式:KAl(SO4)2·12H2O
【答案】B
【解析】
A、氯离子的核电荷数为17,最外层达到8电子稳定结构;B、四氯化碳分子中,Cl原子最外层满足8电子稳定结构;C、甲烷含有C-H键,为正四面体结构;D、明矾的化学式:KAl(SO4)2·12H2O
A、氯离子的核电荷数为17,最外层达到8电子稳定结构;氯离子的结构示意图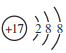 ,故A正确;B、氯原子未成键的孤对电子对未标出,四氯化碳正确的电子式为
,故A正确;B、氯原子未成键的孤对电子对未标出,四氯化碳正确的电子式为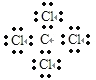 ,故B错误;C、甲烷含有C-H键,为正四面体结构,球棍模型为
,故B错误;C、甲烷含有C-H键,为正四面体结构,球棍模型为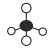 ,故C正确;D、明矾是一种常见的净水剂,明矾的化学式:KAl(SO4)2·12H2O,故D正确;故选B。
,故C正确;D、明矾是一种常见的净水剂,明矾的化学式:KAl(SO4)2·12H2O,故D正确;故选B。

练习册系列答案
相关题目
【题目】物质A~E均含同种元素,都是中学化学中常见的物质,C为蓝色不溶于水的固体,它们可发生如下图所表示的反应(除A~E外的其他物质已略去):

(1)写出相应物质的类别:
物质 | B | C | D |
类别 | ___________ | ______________ | ______________ |
(2)在以上反应中(用序号填空):
属于氧化还原反应的是________;属于复分解反应的是________。
(3)写出反应③和⑦的离子方程式:_______________________。