��Ŀ����
����Ŀ�����Ȼ���������([Co(NH3)6]Cl3)��һ�ֳȻ�ɫ���壬ʵ�����Ʊ��������£�
����ϸ��6 g CoCl26H2O�����4 g NH4Cl���������ƿ�У���ˮ�������ܽ⣬��ȴ��
����13.5 mLŨ��ˮ���û���̿����������Ͼ��Ⱥ���εμ�13.5 mL 5% H2O2��Һ��ˮԡ������50~60�棬����20 min���ñ�ԡ��ȴ�����ˣ��ôֲ�Ʒ��
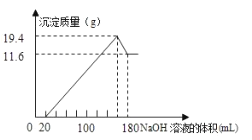
���ֲ�Ʒ����50 mL�ȵ�ϡ�����У�______������Һ�л�������6.7 mLŨ���ᣬ�д����Ȼ�ɫ������������ԡ��ȴ����ˣ�
�����������2 mol��L1 HCl��Һϴ�Ӿ��壬���������Ҵ�ϴ�ӣ�����ò�Ʒ��
(1)[Co(NH3)6]Cl3��Co�Ļ��ϼ���______��
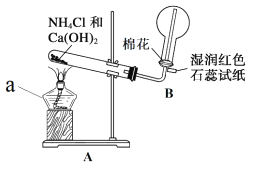
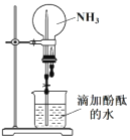
(2)CoCl2��Ũ��ˮ����Co(OH)2����������Ũ��ˮǰ�ȼ���NH4Cl�ɱ���������ɣ�ԭ����______��
(3)��Һ��CoCl2��NH4Cl��Ũ��ˮ��Ϻ���H2O2��Һ��Ӧ����[Co(NH3)6]Cl3�Ļ�ѧ����ʽ��______��
(4)��ȫ���еIJ�����______��
(5)�����ζ����ⶨ�Ʊ��IJ�Ʒ��Cl��������������
����ȷ��ȡa g ���еIJ�Ʒ�����Ƴ�100 mL��Һ����ȡ25 mL��Һ����ƿ�У�
�����μ�����0.005 mol��L1 K2CrO4��Һ��Ϊָʾ������c mol��L1 AgNO3��Һ�ζ����յ㣻
����ƽ�вⶨ���Σ�����AgNO3��Һ�������ƽ��ֵΪv mL�����㾧����Cl��������������
��֪���ܽ�ȣ�AgCl 1.3��106 mol��L1��Ag2CrO4(ש��ɫ)6.5��105 mol��L1
�٢��У��ζ����յ��������______��
���Ʊ��ľ�����Cl��������������______(�м���ʽ��Cl�����ԭ��������35.5)��
���𰸡�+3 ![]() ����NH3��H2O�ĵ��룬ʹ��Һ�е�c(OH��)���ͣ���������Co(OH)2���� 2CoCl2+10NH3��H2O+2NH4Cl+H2O2
����NH3��H2O�ĵ��룬ʹ��Һ�е�c(OH��)���ͣ���������Co(OH)2���� 2CoCl2+10NH3��H2O+2NH4Cl+H2O2![]() 2[Co(NH3)6]Cl3+12H2O ���ȹ��ˡ���ȴ ��Һ�г���ש��ɫ������������ڲ���ʧ
2[Co(NH3)6]Cl3+12H2O ���ȹ��ˡ���ȴ ��Һ�г���ש��ɫ������������ڲ���ʧ ![]()
��������
�������⣬�ڰ������Ȼ�林��������£��Ի���̿Ϊ��������˫��ˮ����CoCl2��Һ���Ʊ� [Co(NH3)6] Cl3����Ӧ�Ļ�ѧ����ʽΪ2CoCl2+10NH3��H2O+2NH4Cl+H2O2![]() 2[Co(NH3)6]Cl3+12H2O�����ֲ�Ʒ����50 mL�ȵ�ϡ�����У�������Һ�л�������6.7 mLŨ���ᣬ�д����Ȼ�ɫ������������ԡ��ȴ����ˣ�˵�������ȵ�ϡ�����Ӧ���ˣ��������2 mol��L1 HCl��Һϴ�Ӿ��壬���������Ҵ�ϴ�ӣ�����ò�Ʒ��
2[Co(NH3)6]Cl3+12H2O�����ֲ�Ʒ����50 mL�ȵ�ϡ�����У�������Һ�л�������6.7 mLŨ���ᣬ�д����Ȼ�ɫ������������ԡ��ȴ����ˣ�˵�������ȵ�ϡ�����Ӧ���ˣ��������2 mol��L1 HCl��Һϴ�Ӿ��壬���������Ҵ�ϴ�ӣ�����ò�Ʒ��
(1). [Co(NH3)6]Cl3��NH3Ϊ���壬�ȵĻ��ϼ�Ϊ-1�ۣ���Co�Ļ��ϼ���+3�ۣ��ʴ�Ϊ+3��
(2).����NH4Clʹ��Һ�е�![]() Ũ������
Ũ������![]() ����NH3��H2O�ĵ��룬ʹ��Һ�е�c(OH��)���ͣ���������Co(OH)2�������ʴ�Ϊ��
����NH3��H2O�ĵ��룬ʹ��Һ�е�c(OH��)���ͣ���������Co(OH)2�������ʴ�Ϊ��![]() ����NH3��H2O�ĵ��룬ʹ��Һ�е�c(OH��)���ͣ���������Co(OH)2������
����NH3��H2O�ĵ��룬ʹ��Һ�е�c(OH��)���ͣ���������Co(OH)2������
(3).�ɷ�����֪����Һ��CoCl2��NH4Cl��Ũ��ˮ��Ϻ���H2O2��Һ��Ӧ����[Co(NH3)6]Cl3�Ļ�ѧ����ʽ��CoCl2+10NH3��H2O+2NH4Cl+H2O2![]() 2[Co(NH3)6]Cl3+12H2O���ʴ�Ϊ��CoCl2+10NH3��H2O+2NH4Cl+H2O2
2[Co(NH3)6]Cl3+12H2O���ʴ�Ϊ��CoCl2+10NH3��H2O+2NH4Cl+H2O2![]() 2[Co(NH3)6]Cl3+12H2O��
2[Co(NH3)6]Cl3+12H2O��
(4).�ɷ�����֪���ڢ���ȱ�ٲ����ǹ��ˣ��������ڼ����ȵ�ϡ����ʴ�Ϊ�����ȹ��ˡ���ȴ��
(5).�������֪��AgCl���ܽ��С��Ag2CrO4����Һ�ȣ������ڵμ�AgNO3ʱAg+����Cl-��Ӧ����AgCl��������Cl-������ʱ����CrO42-��ϣ����Եζ��յ�ʱ��Ag+��CrO42-�������ש��ɫ���� ���ʴ�Ϊ����Һ�г���ש��ɫ������������ڲ���ʧ��
����AgCl�����Ļ�ѧʽ��֪����ӦʱAg+��Cl-���ʵ���֮��Ϊ1:1���ζ�ʱ����AgNO3�����ʵ���Ϊcmol/L��vmL��10-3=cv��10-3mol����25ml��Һ��Cl-���ʵ���Ϊcv��10-3mol��25ml��Һ��Cl-������Ϊ��m=n��M=cv��10-3mol��35.5g/mol=35.5 cv��10-3g����100g��Һ��Cl-������Ϊ��4��35.5 cv��10-3g������������Ϊ��![]() ���ʴ�Ϊ
���ʴ�Ϊ![]() ��
��