题目内容
【题目】现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
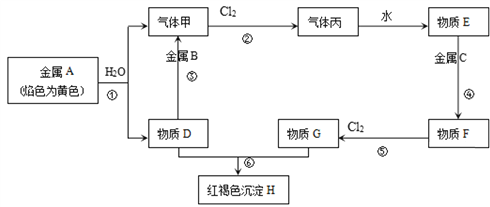
请回答下列问题:
(1)写出下列物质的化学式:B_____________、丙____________;
(2)写出下列反应的化学方程式;
反应①_________________________________________________________________;
反应③_________________________________________________________________;
反应⑤_________________________________________________________________;
(3)向F的溶液中加入D溶液后产生的现象是________________________________,并用化学反应方程式解释产生此现象的原因____________________、_________________。
【答案】Al HCl2Na+2H2O=2NaOH+H2↑2Al+2NaOH+2H2O2NaAlO2+3H2↑2FeCl2+Cl2=2FeCl3先变成白色沉淀,然后迅速变成灰绿色,最后变成红褐色沉淀FeCl2 +2NaOH=Fe(OH)2↓+2NaCl4Fe(OH)2+O2+2H2O===4Fe(OH)3
【解析】
金属A焰色反应为黄色证明为Na,与水反应生成气体甲为H2,D为NaOH;金属B和氢氧化钠溶液反应,说明B为Al,气体甲和氯气反应生成丙为HCl,物质E为盐酸溶液,物质D氢氧化钠和物质G为反应生成红褐色沉淀H为Fe(OH)3,G为FeCl3,推断物质F为FeCl2,C为Fe。(1)由上述分析可知, B的化学式为:Al、丙的化学式为:HCl;(2)反应①的化学方程式为:2Na+2H2O=2NaOH+H2↑;反应③的化学方程式为:2Al+2NaOH+2H2O2NaAlO2+3H2↑;反应⑤的化学方程式为:2FeCl2+Cl2=2FeCl3;(3)向FeCl2的溶液中加入NaOH溶液后产生的现象是:先变成白色沉淀,然后迅速变成灰绿色,最后变成红褐色沉淀;发生反应的化学方程式为:FeCl2 +2NaOH=Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O=4Fe(OH)3。