题目内容
【题目】乙酸甲酯的催化醇解反应可用于制备甲醇和乙酸已酯,该反应的化学方程式为:CH3COOCH3(l)+C6H13OH(l)![]() CH3COOC6H13(l)+CH3OH(l)
CH3COOC6H13(l)+CH3OH(l)
已知v正=k正·x(CH3COOCH3)·x(C6H13OH),v逆=k逆·x(CH3COOC6H13)·x(CH3OH),其中k正、k逆为速率常数(受温度影响),x为各组分的物质的量分数。反应开始时,CH3COOCH3和C6H13OH按物质的量之比1:1投料,测得338K、343K、348K三个温度下CH3COOCH3转化率(α)随时间(t)的变化关系如图所示。下列说法正确的是( )
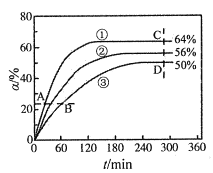
A.该反应的△H>0
B.348K时,该反应的平衡常数为1.8
C.A、B、C、D四点中,v正最大的是D
D.在曲线①、②、③中,k正-k逆最大的曲线是①
【答案】AD
【解析】
A.根据图像,①的反应速率最快,说明①对应的是最高温度348K,温度升高,平衡时转化率增大,说明正向是吸热的,所以ΔH>0;A选项正确;
B.348K时,设初始投入为1mol,则有:

带入平衡常数表达式:![]() =
= ![]() ,B选项错误;
,B选项错误;
C.A点x(CH3COOCH3)·x(C6H13OH)大且温度高,所以A点v正最大,C选项错误;
D.k正、k逆为速率常数,根据平衡移动规律,k正受温度影响更大,因此温度升高,k正的增大程度大于k逆,因此,k正-k逆值最大的曲线是①,D选项正确;
答案选AD。

【题目】某温度下,在甲、乙、丙、丁四个恒容密闭容器中通入 H2 和 I2,发生反应:H2(g)+I2(g)![]() 2HI(g)。反应体系中各物质浓度的有关数据如下。
2HI(g)。反应体系中各物质浓度的有关数据如下。
容器 | 起始浓度 | 平衡浓度 | |
c(H2)/molL-1 | c(I2)/molL-1 | c(HI)/molL-1 | |
甲 | 0.01 | 0.01 | 0.004 |
乙 | 0.01 | 0.02 | a |
丙 | 0.02 | 0.01 | b |
丁 | 0.02 | 0.02 | — |
下列判断正确的是
A.HI 的平衡浓度:a=b>0.004
B.平衡时,H2 的平衡转化率:丁>甲
C.平衡时,乙中 H2 的平衡转化率等于 20%
D.丙中条件下,该反应的平衡常数 K=4
【题目】化学反应速率和化学反应的限度是化学反应原理的重要组成部分。
(1)探究反应条件对0.10mol/LNa2S2O3溶液与0.10mol/L 稀H2SO4反应速率的影响。反应方程式为:Na2S2O3 +H2SO4=Na2SO4+S↓+SO2↑+H2O。设计测定结果如下:
编号 | 反应温度/℃ | Na2S2O3溶液/mL | 甲/mL | H2SO4溶液/mL | 乙 |
① | 25 | 10.0 | 0 | 10.0 | x |
② | 25 | 5.0 | A | 10.0 | y |
③ | 0 | 10.0 | 0 | 10.0 | z |
若上述实验①②是探究浓度对化学反应速率的影响,则a为____________,乙是实验需要测量的物理量,则表格中“乙”为____________,x、y、z的大小关系是____________。
(2)氨气具有广泛的用途,工业上合成氨的反应是N2(g)+3H2(g)=2NH3(g).
①已知:
化学键 | H-H | N≡N | N-H |
键能kJ/mol(断开1mol化学键所需要的能量) | 436 | 945 | 391 |
则合成氨的热化学方程式是________________________________________。
②若反应起始时N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.1mol/L,达到平衡时NH3浓度的范围是____________________。
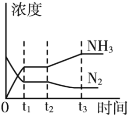
③如图表示该反应在t1时刻达到化学平衡,在t2时因改变某个条件而发生变化的情况,则t2时刻改变条件可能是__________。