题目内容
【题目】可逆反应mA(g)nB(g)+pC(s)△H=Q,温度和压强的变化对正、逆反应速率的影响分别符合图中的两个图象,以下叙述正确的是( ) 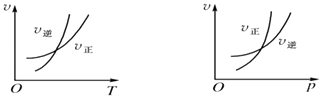
A.m>n,Q>0
B.m>n+p,Q>0
C.m>n,Q<0
D.m>n+p,Q>0
【答案】C
【解析】解:由第一个图可知,在交叉点后升高温度逆反应速率大于正反应速率,则升高温度、平衡逆向移动,可知正反应为放热反应,即Q<0;由第二个图可知,在交叉点后压强增大正反应速率大于逆反应速率,则增大压强,平衡正向移动,可知该反应为气体体积减小的反应,C为固体,即m>n,
故选C.
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)).

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
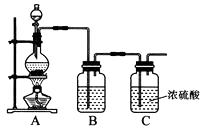
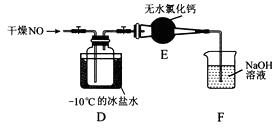
金博士一点全通系列答案【题目】1774年瑞典化学家舍勒用软锰矿(主要成分是二氧化锰)和盐酸共热得到黄绿色气体.甲、乙两个同学分别采取上述反应原理,各制取一瓶氯气,并用其验证Cl2与水反应所得产物的性质.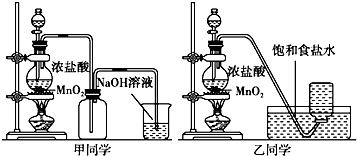
请回答:
(1)写出实验室制备氯气的化学方程式 .
(2)对于乙同学的实验装置,若要停止实验,其操作顺序是 . ①停止加热 ②取出集气瓶盖好 ③将导管伸入到烧碱溶液中
(3)甲、乙两同学分别向收集到的氯气中加入适量水,充分振荡后分成两份,均做验证氯气与水反应所得产物性质的两个实验.实验操作、现象、结论记录如下:
实验序号 | 实验操作 | 现象 | 结论 |
① | 加品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
② | 加入NaHCO2粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
请你填写下表评价甲、乙同学实验①、②的结论(填合理或不合理)
实验序号 | 甲 | 乙 |
① | ||
② |
(4)丙同学查阅资料发现HClO的氧化性大于MnO2 , 拟用下列四组试剂在实验室制取氧气A.CaC12和次氯酸B.浓盐酸NaClO
C.浓盐酸和次氯酸 D.固体NaCl、固体NaClO和浓硫酸
你认为上述四种试剂中组试剂符合实际,且Cl的原子利用率最高.试写出这个反应的化学方程式 .