题目内容
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系
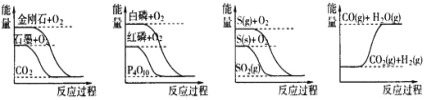
据此判断下列说法中正确的是( )
A. 石墨转变为金刚石是吸热反应
B. 白磷比红磷稳定
C. ①S(g)+O2(g)=SO2(g);②S(s)+O2(g)=SO2(g);放出热量:①②
D. CO(g)+H2O(g)=CO2(g)+ H2 (g);该反应为吸热反应
【答案】A
【解析】
A.由图像可知金刚石所具有的总能量比石墨高,因此石墨转变为金刚石是吸热反应,故A项正确;B.由图像可知红磷所具有的能量比白磷低,因此红磷更稳定,故B项错误;C.对同一种物质而言,气态时所具有的能量比固态时所具有有能量高,即S(g)所具有的能量大于S(s),放出热量应该为①>②,故C项错误;D.由图像可CO(g)和H2O(g)所具有的总能量高于CO2(g)和 H2 (g)所具有的总能量,因此反CO(g)+H2O(g)=CO2(g)+ H2 (g)为放热反应,故D项错误;答案选A。

【题目】(1)结合表中给出的电离平衡常数回答下列问题:
酸或碱 | CH3COOH | HNO2 | HCN | HClO |
电离平衡常数(Ka或Kb) | 1.8×10-5 | 4.6×10-4 | 5×10-10 | 3×10-8 |
①上述四种酸中,酸性最弱、最强的酸分别是_______、_______(用化学式表示)。
②下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是____(填序号)。
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体
D.加少量冰醋酸 E.加氢氧化钠固体
③依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式___________________________________。
(2) 某学习小组利用酸性KMnO4和H2C2O4反应来探究“外界条件对化学反应速率的影响”。 实验时,先分别量取KMnO4酸性溶液、H2C2O4溶液,然后倒入大试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。
①已知草酸H2C2O4是一种二元弱酸,写出草酸的电离方程式__________、___________。酸性KMnO4溶液和H2C2O4溶液反应的离子方程式为:_____________________________
某同学设计了如下实验
实验编号 | H2C2O4溶液 | KMnO4溶液 | 温度/℃ | ||
浓度(mol/L) | 体积(mL) | 浓度(mol/L) | 体积(mL) | ||
a | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
b | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
c | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
②探究浓度对化学反应速率影响的组合实验编号是__________,可探究温度对化学反应速率影响的实验编号是__________。
③实验a测得混合后溶液褪色的时间为40 s,忽略混合前后体积的微小变化,则这段时间内的平均反应速率v(KMnO4)=______ mol·L-1·min-1。
④在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快,其可能的原因是___________________________________
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
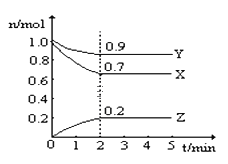
(1)该反应的化学方程式为 _______________________。
(2)从开始至2min,Z的平均反应速率为 ___________。
(3)某探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如下表所示:
实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
Ⅰ | 薄片 | 15 | 200 |
Ⅱ | 薄片 | 25 | 90 |
Ⅲ | 粉末 | 25 | 10 |
①该实验的目的是探究 ______ 、 ______ 对锌和稀盐酸反应速率的影响;
②实验Ⅰ和Ⅱ表明 ________________________________ ,化学反应速率越大;
③能表明固体的表面积对反应速率有影响的实验编号是 ______ 和 ______;
④请设计一个实验方案证明盐酸的浓度对该反应的速率的影响: ______________________。