题目内容
19.随着碱金属、卤素原子半径的增大,下列递变规律正确的是( )| A. | 碱金属和卤素单质的熔沸点都逐渐降低 | |
| B. | 碱金属和卤素单质的密度都依次变大 | |
| C. | 卤素的气态氢化物稳定性逐渐增强 | |
| D. | 碱金属单质还原性逐渐增强 |
分析 A.卤素单质的熔沸点随着原子半径增大而升高;
B.钠的密度大于钾的密度;
C.元素的非金属性越强,其气态氢化物越稳定;
D.同主族从上到下金属性增强、还原性增强.
解答 解:A.卤素单质是分子晶体,分子晶体的熔沸点与其相对分子质量成正比,所以卤素单质的熔沸点随着原子半径增大而升高,碱金属单质的熔沸点逐渐降低,故A错误;
B.碱金属和卤素单质的密度都依次变大,但是钠钾反常,钠的密度大于钾的密度,故B错误;
C.非金属性随着原子半径增大而减弱,所以气态氢化物的稳定性随着原子半径增大而逐渐减弱,故C错误;
D.同主族从上到下金属性增强、还原性增强,则碱金属单质还原性逐渐增强,故D正确;
故选D.
点评 本题以碱金属族、卤族元素为例考查同一主族元素性质递变规律,同时考查学生灵活运用知识能力,题目难度不大.

练习册系列答案
相关题目
9.能使酸性高锰酸钾溶液褪色而不能使溴水褪色的烃是( )
| A. | CH2=CH-CH2-CH2-CH2-CH3 | B. | HC≡C-CH2-CH2-CH2-CH3 | ||
| C. |  | D. | 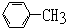 |
4.下列说法正确的是( )
①一块冰中氢、氧原子间只以化学键相结合
②金属和非金属化合形成离子键
③离子键是阳离子、阴离子的相互吸引
④双原子单质分子中的共价键一定是非极性键
⑤非金属原子间不可能形成离子键
⑥离子化合物中可能有共价键
⑦共价化合物中可能有离子键
⑧两种不同非金属元素形成的共价化合物中只有极性键.
①一块冰中氢、氧原子间只以化学键相结合
②金属和非金属化合形成离子键
③离子键是阳离子、阴离子的相互吸引
④双原子单质分子中的共价键一定是非极性键
⑤非金属原子间不可能形成离子键
⑥离子化合物中可能有共价键
⑦共价化合物中可能有离子键
⑧两种不同非金属元素形成的共价化合物中只有极性键.
| A. | ④⑥ | B. | ②④⑤ | C. | ①②③ | D. | ④⑥⑧ |
5.能清楚地反映甲烷分子里碳、氢原子的大小和相对位置的是( )
| A. | 结构式 | B. | 电子式 | C. | 球棍模型 | D. | 比例模型 |
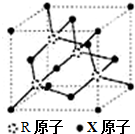 X、Y、Z、R为短周期元素,原子序数依次增大.X的基态原子的s能级电子数是p能级电子数的2倍;Y的单质在空气中含量最高;Z的氧化物是常见的两性氧化物;R基态原子最外层成对电子的数目和未成对电子的数目相等.
X、Y、Z、R为短周期元素,原子序数依次增大.X的基态原子的s能级电子数是p能级电子数的2倍;Y的单质在空气中含量最高;Z的氧化物是常见的两性氧化物;R基态原子最外层成对电子的数目和未成对电子的数目相等.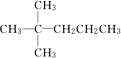 ,并对其命名2,2-二甲基戊烷.其中另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称3,3-二甲基-1-戊烯.
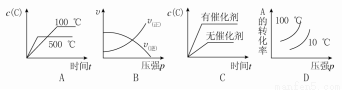
,并对其命名2,2-二甲基戊烷.其中另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称3,3-二甲基-1-戊烯. 2C(g)ΔH<0,下列图象正确的是
2C(g)ΔH<0,下列图象正确的是