题目内容
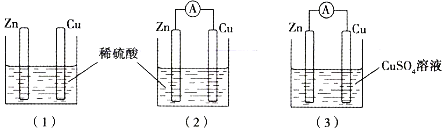
【题目】将图Ⅰ所示装置通电10 min后,撤掉直流电源,连接成图Ⅱ所示装置,可观察到U形管左侧铁电极表面析出了白色胶状物质,U形管右侧液面上升。下列说法正确的是( )

A. 同温同压下,装置Ⅰ中石墨电极上方得到的气体比铁电极上方得到的气体多
B. 装置Ⅱ中铁电极的电极反应式为Fe-2e-+2OH-===Fe(OH)2↓
C. 装置Ⅱ中石墨电极的电极反应式为2H++2e-===H2↑
D. 装置Ⅰ通电10 min后,铁电极附近溶液的pH降低
【答案】B
【解析】
A.装置Ⅰ中石墨电极与电源的正极相连,作阳极,氯离子放电生成Cl2,铁电极是阴极,氢离子放电,生成H2,因Cl2能溶解在水中,且与H2O发生反应:Cl2+H2O=HCl+HClO,而H2不溶于水,故石墨电极上方得到的气体比铁电极上方得到的气体少,A错误;
B.装置Ⅱ是原电池装置,Fe为负极,失去电子产生Fe2+,溶液显碱性,Fe2+再与溶液中的OH-反应生成Fe(OH)2:Fe-2e-+2OH-=Fe(OH)2↓,B正确;
C.装置Ⅱ是原电池装置,石墨为正极,正极为Cl2得到电子:Cl2+2e-=2Cl-,C错误;
D.装置Ⅰ中铁电极是阴极,氢离子放电产生H2:2H2O+2e-=H2↑+2OH-,由于有OH-生成,故溶液的pH升高,D错误。
答案选B。

【题目】在一定条件下有反应:2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ/mol.现有容积相同的甲、乙、丙三个定容容器。在上述条件下分别充入的气体和反应放出的热量(Q)如表所示:
2SO3(g) △H=-197kJ/mol.现有容积相同的甲、乙、丙三个定容容器。在上述条件下分别充入的气体和反应放出的热量(Q)如表所示:
容器 | SO2(mol) | O2(mol) | N2(mol) | Q(kJ) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | Q2 |
丙 | 1 | 0.5 | 1 | Q3 |
根据以上数据,下列叙述不正确的是:
A. Q1<197
B. 在上述条件下,反应生成1molS03气体放热98.5kJ
C. Q2=Q3
D. Q3<Q1<2Q2