��Ŀ����
15����֪a��b�������Ӻ�c��d�������ӵ��Ӳ�ṹ��ͬ����ԭ�Ӱ뾶a��b�����������������c��d�������ǵ�ԭ��������ϵ�ǣ�������| A�� | c��d��a��b | B�� | a��b��d��c | C�� | b��a��d��c | D�� | b��a��c��d |
���� a��b�������Ӻ�c��d�������ӵ��Ӳ�ṹ��ͬ�������Ӻ����������ȣ�a��bͬ���ڣ�c��dͬ���ڣ���a��b����c��d����һ���ڣ�ͬ�����������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶a��b����֪ԭ������a��b�����������������c��d����ԭ������c��d��
��� �⣺a��b�������Ӻ�c��d�������ӵ��Ӳ�ṹ��ͬ�������Ӻ����������ȣ�a��bͬ���ڣ�c��dͬ���ڣ���a��b����c��d����һ���ڣ���a��bԭ������������c��d��
ͬ�����������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶a��b����֪ԭ������a��b��
���������������c��d����ԭ������c��d��
��ԭ������b��a��d��c��
��ѡC��
���� ���⿼��ԭ�ӽṹ��Ԫ��������֪ʶ����Ŀ�ѶȲ��ؼ����ƶ�Ԫ�����������е����λ�ã������ڻ���֪ʶ�Ĺ��̣�

��ϰ��ϵ�д�
�����Ŀ
6�����в��ֶ�����Ԫ�ص����ʻ�ԭ�ӽṹ���±���
��1��д��Ԫ��X�����ӽṹʾ��ͼ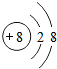 ��д��Ԫ��Z�ĵ��ʵĵ���ʽ
��д��Ԫ��Z�ĵ��ʵĵ���ʽ ����Ԫ�ط��ű�ʾ��
����Ԫ�ط��ű�ʾ��
��2��д��YԪ�ص�����������ˮ�ĵ��뷽��ʽAl2��SO4��3�T2Al3++3SO42-��
��3��Ԫ��T�����ڱ��е�λ���ǵڶ����ڢ���A�壻���б����ܱȽ�T����Ԫ�طǽ�����ǿ������ʵ��cd
a����������������ɫ��T���ʵ���ɫ��
b��T�ĵ���ͨ���Ȼ���ˮ��Һ�����û�������
c������T�γɵĻ���������Ԫ�س�����̬
d��T����̬�⻯����Ȼ����ȶ���
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
| T | ��������ˮ���ҷ�Ӧ��������Һ�������� |
| X | ԭ�������������Ǵ�����3�� |
| Y | ��������Ԫ�صļ������а뾶��С |
| Z | ��̬�⻯��������������Ӧˮ����ɷ������Ϸ�Ӧ |
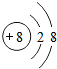 ��д��Ԫ��Z�ĵ��ʵĵ���ʽ
��д��Ԫ��Z�ĵ��ʵĵ���ʽ ����Ԫ�ط��ű�ʾ��
����Ԫ�ط��ű�ʾ����2��д��YԪ�ص�����������ˮ�ĵ��뷽��ʽAl2��SO4��3�T2Al3++3SO42-��
��3��Ԫ��T�����ڱ��е�λ���ǵڶ����ڢ���A�壻���б����ܱȽ�T����Ԫ�طǽ�����ǿ������ʵ��cd
a����������������ɫ��T���ʵ���ɫ��
b��T�ĵ���ͨ���Ȼ���ˮ��Һ�����û�������
c������T�γɵĻ���������Ԫ�س�����̬
d��T����̬�⻯����Ȼ����ȶ���
3���ȿ�����������������Ȳ���ֿ���������ȥ�����л��е���Ȳ���壬�õ������ļ���ķ����ǣ�������
| A�� | ͨ��������ˮ | |
| B�� | ͨ�����������Ը��������Һ | |
| C�� | ȼ�� | |
| D�� | ʹ��Ȳ��һ�������������������ӳɷ�Ӧ |
10��ijԪ�ص�����ͬλ�أ����ǵ�ԭ�Ӿ��в�ͬ�ģ�������
| A�� | ������ | B�� | ������ | C�� | ԭ������ | D�� | ������ |
20��2010�����粩������2010��5��1����10��31�����й��Ϻ����У�Ϊ�˹᳹��̬����������ɫ������������д�ʩ�в��������ǣ�������
| A�� | �����������д��ģ�̻����裬����̻���� | |
| B�� | �����յ�����ˮ��������ˮ�ռ�ϵͳ���������ˮ��Դ | |
| C�� | ���������������ռ��������м��з��մ��� | |
| D�� | �ڽ�������չ����Ӫ������Ӧ�ô��ģ��̫���ܹ������ϵͳ |
7���������ʵĵ���ʽ������ǣ�������
| A�� | CaCl2 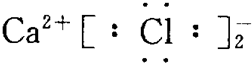 | |
| B�� | Na2O  | |
| C�� | NaCl 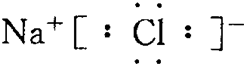 | |
| D�� | H2O  |
4��������Ԫ��W��X��Y��Z��ԭ������������������W�������ӵĺ����������X��Y��Zԭ�ӵĺ����ڲ��������ͬ��X��һ�ֺ����ڿ���ʱ����������һЩ������������ҵ�ϲ���Һ̬��������������Y�ĵ��ʣ���Z�����γ�˫ԭ�ӷ��ӣ�������������������˵����ȷ���ǣ�������
| A�� | ��������Ԫ�ص�ԭ�Ӱ뾶��СΪW��X��Y��Z | |
| B�� | W��X��Y��Zԭ�ӵĺ����������������ܺ�Ϊ20 | |
| C�� | W��Y���γɼȺ����Թ��ۼ��ֺ��зǼ��Թ��ۼ��Ļ����� | |
| D�� | XW4һ������YW3���ȶ��� |
 ��
��