题目内容
13.用铝制易拉罐收集满CO2,加入过量NaOH浓溶液,立即把口封闭.发现易拉罐“咔咔”作响并变瘪了,过了一会儿,易拉罐又会作响并鼓起来,下列说法正确的是( )| A. | 导致易拉罐变瘪的离子反应是CO2+OH-=HCO3- | |
| B. | 导致易拉罐又鼓起来的反应是Al3++3HCO3-=Al(OH)3+3CO2↑ | |
| C. | 上述过程中共发生了三个化学反应,且反应结束后的溶液呈碱性 | |
| D. | 若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象 |
分析 易拉罐变瘪发生CO2+2OH-═CO32-+H2O,气体的压强变小;过一会儿后,易拉罐又会作响并鼓起来,发生2Al+2OH-+2H2O═2AlO2-+3H2↑,气体压强增大,以此来解答.
解答 解:A.气体与碱反应,导致易拉罐变瘪,反应为CO2+2OH-═CO32-+H2O,故A错误;
B.易拉罐又会作响并鼓起来,发生2Al+2OH-+2H2O═2AlO2-+3H2↑,气体压强增大,故B错误;
C.上述过程共发生CO2+2OH-═CO32-+H2O、2Al+2OH-+2H2O═2AlO2-+3H2↑、Al2O3+2NaOH=2NaAlO2+H2O反应,反应后溶液显碱性,故C正确;
D.将CO2换为NH3,浓NaOH溶液换为水,只发生氨气与水反应,则易拉罐也会出现变瘪的现象,故D错误;
故选C.
点评 本题考查Al的化学性质及离子反应,为高频考点,明确发生的化学反应是解答本题的关键,题目难度不大,选项C为解答的难点,侧重分析与知识应用能力的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.常温下,下列关于电解质溶液的说法正确的是( )
| A. | pH=4的CH3COOH溶液加水稀释10倍,溶液中各离子浓度均减小 | |
| B. | 用CH3COOH溶液滴定等浓度的NaOH至pH=7,V(CH3COOH溶液)<V(NaOH溶液) | |
| C. | 向0.2moj/L的盐酸中加入等体积0.1mol/L氨水溶液:c(Cl-)+c(OH-)=c(H+)+c(NH3••H2O) | |
| D. | 在含0.1mol NaHSO4溶液中:c(H+)=c(SO42-)+c(OH-) |
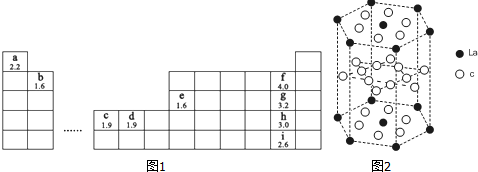
4.如图1为元素周期表的一部分,字母下方数值为该元素电负性,根据信息回答下列问题(用相应元素符号进行答题):
(1)b、h两元素可形成化合物bh2,写出其电子式: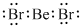 .
.
(2)e、g两元素可形成两种化合物eg3、e2g6,eg3的分子构型为平面正三角形,eg3、e2g6中心原子e的杂化方式分别为sp2、sp3.
(3)d元素形成的单质可与g的氢化物浓溶液在加热条件下反应生成一种以二价d离子为内界中心原子(配位数为4)的配位化合物与一种可燃性气体,写出反应的化学方程式:Cu+4HCl=H2CuCl4+H2↑.
(4)f、g、h、i四种元素对应单质分子的键能如下表:
试从原子半径角度阐述f-f键键能反常的原因:F原子半径较小,价电子较多,导致电子云密度增大,极大增加了两原子间的排斥作用,故键能较小,共价键易断裂.
(5)c元素的元素符号是Ni,价电子排布式为3d84s2,下图是一种受到较多关注的c元素单质与金属镧(La)形成的储氢材料的结构示意图,请在图2中勾画出该晶体的一个晶胞.计算出该合金的化学式为:LaNi5.

(1)b、h两元素可形成化合物bh2,写出其电子式:
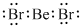 .
.(2)e、g两元素可形成两种化合物eg3、e2g6,eg3的分子构型为平面正三角形,eg3、e2g6中心原子e的杂化方式分别为sp2、sp3.
(3)d元素形成的单质可与g的氢化物浓溶液在加热条件下反应生成一种以二价d离子为内界中心原子(配位数为4)的配位化合物与一种可燃性气体,写出反应的化学方程式:Cu+4HCl=H2CuCl4+H2↑.
(4)f、g、h、i四种元素对应单质分子的键能如下表:
| 共价键 | f-f | g-g | h-h | i-i |
| 键能(kJ/mol) | 157 | 242.7 | 193.7 | 152.7 |
(5)c元素的元素符号是Ni,价电子排布式为3d84s2,下图是一种受到较多关注的c元素单质与金属镧(La)形成的储氢材料的结构示意图,请在图2中勾画出该晶体的一个晶胞.计算出该合金的化学式为:LaNi5.
1.下列物质的性质与应用对应关系正确的是( )
| A. | FeCl3溶液显酸性,可用于蚀刻印刷电路板 | |
| B. | Na2CO3溶液显碱性,可用于除锅垢中的硫酸钙 | |
| C. | MgO、Al2O3熔点高,可用于制作耐高温坩埚 | |
| D. | Na、K合金具有强还原性,可用于原子反应堆的导热剂 |
8.化学来源于生活,服务于生活,下列有关叙述正确的是( )
| A. | 生活中钢铁制品生锈主要是由于吸氧腐蚀所致 | |
| B. | 冰箱中使用的含氟制冷剂泄漏后,会增加空气中PM 2.5的含量 | |
| C. | 氯气和活性炭均可作为漂白剂,同时使用可增强漂白效果 | |
| D. | 明矾[KAl(SO4)2•12H2O]溶于水会形成胶体,因此可用于自来水的杀菌消毒 |
18.下列实验设计或操作正确的是( )
| A. | 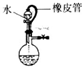 说明该装置气密性良好 | |
| B. | 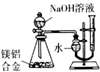 测定镁铝合金中铝的质量分数 | |
| C. | 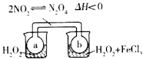 瓶中气体颜色变深,说明H202分解是吸热反应 | |
| D. | 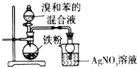 验证苯和溴发生取代反应 |
5.硼和铝是同主族元素,在生产、生活和科研中具有广泛的应用.以下是几种常见的硼化合物:
请回答下列问题:
(1)写出硼元素在周期表中的位置第二周期ⅢA族.
(2)工业上以硼镁矿为原料制取硼,该工艺的中间过程会发生反应:B2O3+3Mg=2B+3MgO,则每生成1mol的硼转移的电子数为3NA.
(3)工业上常用金属铝冶炼难熔金属,请写出以五氧化二矾(V2O5)和铝为原料获得金属矾的化学方程式3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al2O3.
(4)硼酸是一种一元弱酸,它与水作用时结合水电离的OH-而释放出水电离的H+,皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,请写出硼酸与氢氧化钠反应的离子方程式H3BO3+OH-=[B(OH)4]-.
(5)硼氢化钠(NaBH4)是一种强还原剂,遇水剧烈反应产生大量气体,请写出该反应的化学方程式NaBH4+2H2O═NaBO2+4H2↑.
(6)偏硼酸钠能溶于水,其溶液显碱性(填“酸性”、“中性”或“碱性”),原因是BO2-+2H2O?H3BO3+OH-(用离子方程式表示)
| 硼镁矿 | 硼砂 | 硼酸 | 偏硼酸钠 |
| Mg2B2O5•H2O | Na2B4O7•10H2O | H3BO3 | NaBO2 |
(1)写出硼元素在周期表中的位置第二周期ⅢA族.
(2)工业上以硼镁矿为原料制取硼,该工艺的中间过程会发生反应:B2O3+3Mg=2B+3MgO,则每生成1mol的硼转移的电子数为3NA.
(3)工业上常用金属铝冶炼难熔金属,请写出以五氧化二矾(V2O5)和铝为原料获得金属矾的化学方程式3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al2O3.
(4)硼酸是一种一元弱酸,它与水作用时结合水电离的OH-而释放出水电离的H+,皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,请写出硼酸与氢氧化钠反应的离子方程式H3BO3+OH-=[B(OH)4]-.
(5)硼氢化钠(NaBH4)是一种强还原剂,遇水剧烈反应产生大量气体,请写出该反应的化学方程式NaBH4+2H2O═NaBO2+4H2↑.
(6)偏硼酸钠能溶于水,其溶液显碱性(填“酸性”、“中性”或“碱性”),原因是BO2-+2H2O?H3BO3+OH-(用离子方程式表示)
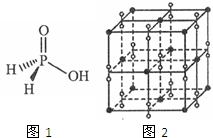 中学化学常见元素氮、磷、钾与氢、氧、卤素等能形成多种化合物.
中学化学常见元素氮、磷、钾与氢、氧、卤素等能形成多种化合物.